1929年Flemingが、青かびの一種Penicillium notatumの培養液中よりPenicillinを発見して以来、微生物は抗生物質をはじめとする医薬品の供給源として、重要な役割をはたしている。 微生物生産物の構造の多様性は、人知の及ばぬところであり、創薬におけるリード化合物探索の有用な資源である。 微生物の産生する生理活性物質の中には、数多くのペプチド化合物が含まれており、その中にはシクロスポリンや、バンコマイシンなど現在臨床の場で重要な役割を担っている化合物も多く存在する。 こうした微生物の産生するペプチドには、N末端がアシル化されたもの、異常アミノ酸やD-アミノ酸を含むもの等、新規骨格を有する化合物が多く、その構造的知見が、医薬品開発に重要な手掛かりを与えることも多い。 したがってこれらの構造を迅速に決定することが、得られた構造をリードとして医薬品を創薬するうえにおいて重要なステップとなってくる。 著者らは1983年来、創薬を目的とした微生物生産物のスクリーニングの過程で、非常に強い薬理作用を有し、かつ新奇な新規環状ペプチド構造を有する天然物、WS9326A、WB2522、およびWS7622Aを見いだす事に成功した。 本論文においては、機器分析並びに化学反応の結果をもとにしたこれら三種の新規環状ペプチドの絶対立体構造解明の化学的研究の成果について論述する。 第一章では抗喘息剤として期待されるニューロキニン受容体拮抗物質のスクリーニングにおいて、ラジオリガンドを用いたバインディングアッセイにより、放線菌Streptomyces violaceusniger No.9326の培養液より見いだされたWS9326Aの構造決定について論述する。 当時の最新の2次元NMR技術(COLOC,ROESY etc)等を駆使した各種機器分析並びに分解反応生成物の構造解析結果をもとにWS9326Aの構造を、新規アミノ酸である(E)- , , -dehydro-N-methyltyrosine((E) -dehydro-N-methyltyrosine((E) MeTyr)および新規カルボン酸である2置換ベンゼン環を有するアシル基を分子内に含む、ユニークなサイクリックヘプタペプチドラクトンであることを明らかとした。この新規アミノ酸である(E) MeTyr)および新規カルボン酸である2置換ベンゼン環を有するアシル基を分子内に含む、ユニークなサイクリックヘプタペプチドラクトンであることを明らかとした。この新規アミノ酸である(E) MeTyrの存在は、還元によりMeTyrが得られたことより確認し、その二重結合の幾何異性はROESYおよび MeTyrの存在は、還元によりMeTyrが得られたことより確認し、その二重結合の幾何異性はROESYおよび -オレフィンプロトンとカルボニル炭素との3JCHカップリング定数によりE配置と決定した。新規アシル側鎖である3-(2-(1-(Z)-pentenyl)phenyl)-2-(E)-propenoic acidの構造は、分解反応、機器分析の結果より推定し、最終的にその合成により確定した。アミノ酸配列は、COLOCおよび、ROESYの結果明らかとし、さらにキラルGC-MSを用いて構成アミノ酸の絶対立体配置を決定した。また分解反応で得られた化合物の構造を明らかとすることにより、L-ThrとL-alloThrの区別を行った。 -オレフィンプロトンとカルボニル炭素との3JCHカップリング定数によりE配置と決定した。新規アシル側鎖である3-(2-(1-(Z)-pentenyl)phenyl)-2-(E)-propenoic acidの構造は、分解反応、機器分析の結果より推定し、最終的にその合成により確定した。アミノ酸配列は、COLOCおよび、ROESYの結果明らかとし、さらにキラルGC-MSを用いて構成アミノ酸の絶対立体配置を決定した。また分解反応で得られた化合物の構造を明らかとすることにより、L-ThrとL-alloThrの区別を行った。 以上の結果、図-1に示すWS9326Aの構造をその絶対構造も含めて決定することができた。  図-1 WS9326Aの構造 図-1 WS9326Aの構造 第二章ではニューロキニン受容体拮抗物質であるWS9326Aの全合成について論述する。 WS9326Aおよびその誘導体からは、X線結晶解析に適した結晶を得ることが出来なかったため、全合成により先に決定した絶対立体構造の確認を試みた。キー反応となる(E) MeTyrの二重結合の導入は、 MeTyrの二重結合の導入は、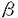 -ヒドロキシアミノ酸の脱離反応にて行ったが、予想に反して目的外のZ配置の立体を持つ化合物しか得られなかった。そこで図-2に示す光化学反応を利用し、この立体を反転させ、目的とするE配置の立体を有するユニットを構築することが出来た。この二重結合の立体は、NOE差スペクトルおよびUVスペクトルより明らかとした。ここで得られた(E)Me -ヒドロキシアミノ酸の脱離反応にて行ったが、予想に反して目的外のZ配置の立体を持つ化合物しか得られなかった。そこで図-2に示す光化学反応を利用し、この立体を反転させ、目的とするE配置の立体を有するユニットを構築することが出来た。この二重結合の立体は、NOE差スペクトルおよびUVスペクトルより明らかとした。ここで得られた(E)Me Tyrユニットを用いてニューロキニンアンタゴニストWS9326Aの全合成に成功した。この結果、構造解析で決定した図-1に示す絶対立体構造が再確認されたとともに、さらに強力なアンタゴニスト合成の可能性が開けた。 Tyrユニットを用いてニューロキニンアンタゴニストWS9326Aの全合成に成功した。この結果、構造解析で決定した図-1に示す絶対立体構造が再確認されたとともに、さらに強力なアンタゴニスト合成の可能性が開けた。 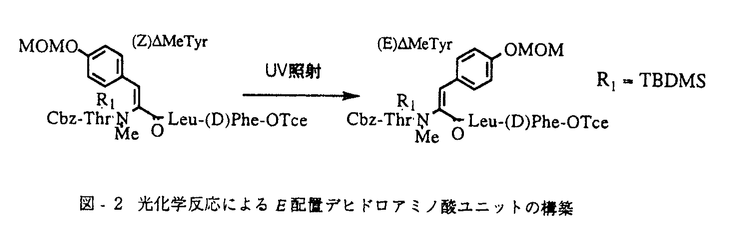 図-2 光化学反応によるE配置デヒドロアミノ酸ユニットの構築 図-2 光化学反応によるE配置デヒドロアミノ酸ユニットの構築 第三章では新らしい作用メカニズムに基づく選択毒性のある夢の抗癌剤を目指し、Ha-ras癌遺伝子形質転換細胞の形態をもとの正常な細胞形態に戻す作用を指標としたスクリーニングの結果、バクテリアPseudomonas chlororaphis No.2522の培養液より得られた抗腫瘍抗生物質WB2522の構造決定について論述する。 各種2次元NMR測定(COLOC,NOESY etc)によりS-S結合を含む特異な2環性のデプシペプチド構造を導きだした。さらにキラルアミノ酸分析ならびにX線結晶解析によりその絶対構造を決定した。その結果、WB2522は図-3に示す分子内にS-S結合を有する2環性のデプシペプチドであることが明らかとなった。 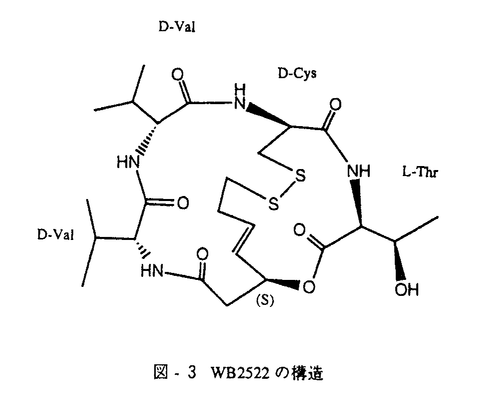 図-3 WB2522の構造 図-3 WB2522の構造 第四章では肺気腫との関連が示唆されている好中球エラスターゼの阻害物質のスクリーニングにより、放線菌Streptomyces resistomycificus No.7622の培養液より得られたWS7622Aの構造決定について論述する。 主に化学分解反応により、新規アミノ酸であるN-Methyl-2’-amino-4’,5’-dihydroxyphenylalanineの構造を確認し、さらにこの2’-アミノ基よりウレア結合でOrnの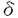 NHが結合することを分解反応物の構造決定により明らかとした。また分子内に3-amino-6-hydroxy-2-piperidone(Ahp)を含む構造であることを化学反応およびNMR解析の結果をもとに推定した。 NHが結合することを分解反応物の構造決定により明らかとした。また分子内に3-amino-6-hydroxy-2-piperidone(Ahp)を含む構造であることを化学反応およびNMR解析の結果をもとに推定した。 アミノ酸配列は、2D NMRの結果のみでは解明できず、分解反応で得られた化合物の構造を明らかとすることにより、その平面構造を導きだした。その結果図-4に示す分子内にウレア結合によるリング並びにラクトンによるリングを持つ2環性のペプチドラクトン構造を明らかとした。キラルGC-MSを用いて既知構成アミノ酸の立体配置を決定した後、最終的な絶対構造は、X線結晶解析により決定した。  図-4 WS7622Aの構造 図-4 WS7622Aの構造 以上著者は、新奇骨格を有する三種の環状ペプチドの構造を、その絶対構造も含めて明らかとした。 微生物は実に巧妙にさまざまな骨格を持つ新奇化合物を作り出しうるものである。著者の最終的な目的は、この天然の恵みを医薬品として役立てることである。今回の構造的知見が今後の医薬品開発に役立つことを期待してやまない。 |