| 内容要旨 | | バクトボラミン(BBL)はPseudomonas属に属する細菌株の抗菌性物質bactobolin(BBN)から誘導された微生物二次代謝産物で,細胞性免疫に対する抑制効果,マウス皮膚移植,ラット肝移植のグラフト生着延長効果についての初期の動物実験の結果がわれわれの研究室から報告されているが,他の免疫抑制剤との効果の比較や他剤との併用効果,副作用などについての検討はまだ行われていない.本研究では以下の実験で,BBLのラット肝移植に対するグラフト生着延長効果,tacrolimus(FK)との併用効果ならびにBBLの副作用について検討した. 1.ラット同種肝移植モデルを用いたBBLの効果の検討 ACI[RT1n]→LEW[RT11]のラット同種肝移植後にBBL50,100,200mg/kg/dayを投与し,mizoribine(MIZ)2.5,5,10mg/kg/dayの効果と比較した.また,FKとの併用投与を行い,MIZとFKの併用効果と比較した.BBLは100mg/mlの濃度で蒸留水に溶解し皮下に投与した.MIZは4.0mg/mlの濃度で生理的食塩水に溶解し,FKは生理的食塩水に0.01mg/mlの濃度で懸濁液として,それぞれ筋肉内に投与した.各薬剤は肝移植後から14日間投与した.BBL単剤投与では,50〜200mg/kg/dayの投与量で肝移植後の平均生存日数は第1群(肝移植後無処置群)よりも有意に(p<0.01),用量依存的に延長した.MIZ単剤投与群の平均生存日数は,5mg/kg/dayの投与量では第1群よりも有意に(p<0.05)延長したが,2.5および10mg/kg/dayの投与量では第1群と有意差はなく,用量依存的な生存日数の延長は得られなかった.FK(0.08mg/kg/day)との併用では,MIZ,BBLともそれぞれ単剤投与の場合と比較して,平均生存日数は有意に延長したが,BBLとFKの併用の方がより有効であった(表1,図1). 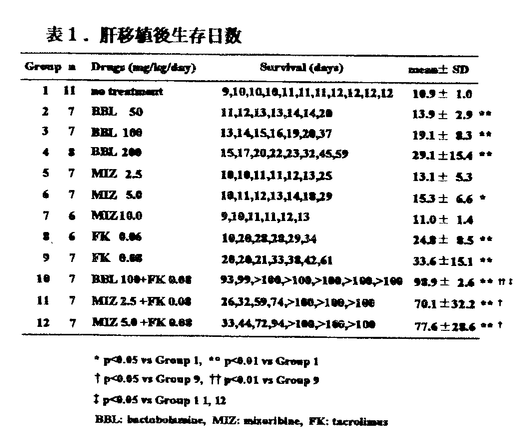 表1.肝移植後生存日数 表1.肝移植後生存日数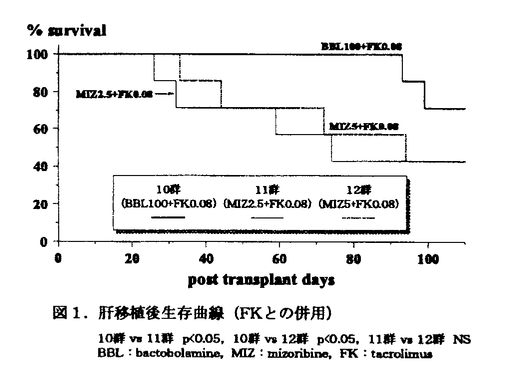 図1.肝移植後生存曲線(FKとの併用) 図1.肝移植後生存曲線(FKとの併用) BBL注射時には立毛や振戦は認めず,また,下痢,嘔吐などの消化器症状も認めなかった.200mg/kg/day投与群では注射部位皮下の浮腫が認められ,8例中5例では皮膚潰瘍も認められた.潰瘍発症例では潰瘍の個数は1〜2個/bodyで,注射部位に毎回発症するものではなかった.BBL100mg/kg/day以下の投与では皮膚潰瘍の発症は認めなかった.MIZ投与群ではBBLと同様に注射時の立毛や振戦は認めなかったが,10mg/kg/day以上の投与で全例に下痢を認めた.肝移植後の体重減少はMIZ投与群と比較してBBL投与群でより軽度で,特に200mg/kg/day投与群では術後10日まで体重減少はほとんど認めなかった. 2.BBLの薬物動態力学検査 正常LEW(9〜10週齢)にBBL200mg/kgを静脈内,皮下または経口投与後,5,10,15,30分,1,2,4,6,24時間後に採血し,BBL血漿中濃度を測定して,血中半減期(elimination half-life;T1/2),最高血漿中濃度(the maximum concentration;Cmax),ピークタイム(time to Cmax;Tmax),濃度-時間経過の曲線下面積(area under the curve;AUC0→∞),生物学的利用率(bioavailability)の薬物動態パラメータを求めた.静脈内投与,皮下投与,経口投与のT1/2(平均±標準偏差)はそれぞれ0.85±0.39,1.82±1.47,1.57±0.52時間であった.静脈内投与の場合のAUCを100としたときのBBLのbioavailabilityは,皮下投与,経口投与でそれぞれ25.9%,14.9%であった.皮下投与と経口投与のAUCの比(AUCsc/AUCpo)は約1.7でBBL200mg/kg皮下投与に相当するBBLの経口投与量は340mg/kgと推定された(表2).  表2.BBL薬物動態パラメータ3.BBL経口投与の有効性の検討 表2.BBL薬物動態パラメータ3.BBL経口投与の有効性の検討 ラット同種肝移植後に,実験2で求めた投与量(340mg/kg/day)のBBLの経口投与を14日間行い,BBLの経口投与での有効性を検討した.BBL経口投与は有効ではあったが,皮下投与ほどの効果は得られなかった. 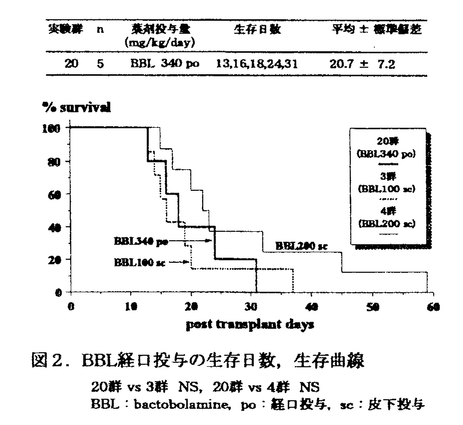 図2.BBL経口投与の生存日数,生存曲線4.BBLの副作用についての検討 図2.BBL経口投与の生存日数,生存曲線4.BBLの副作用についての検討 LEW→LEWのラット同系肝移植後に340mg/kg/dayのBBLを経口投与し,コントロール群(同系肝移植後蒸留水3.4ml/kg/day経口投与)との比較を行った.BBL投与群の術後3,6,9日目の血清TP,T-BIL,GOT,GPT,ALP,Crの各値はいずれもコントロール群の各値との間に有意差を認めなかった.術後9日目の赤血球,白血球数,ヘモグロビン,ヘマトクリットの各値はBBL投与群,コントロール群の間で有意差は認めなかった.BBL投与群の肝,膵,脾,腎,肺,心,胸腺,骨髄(胸骨)の諸臓器の病理組織像は,コントロール群と同様に特に異常所見は認めなかった.胸腺では皮質と髄質の比に変化はみられず,脾臓では白脾髄の萎縮は認めなかった.胃には肉眼的所見でも病理組織所見でもビランその他の異常所見は認めず,BBL経口投与による消化管傷害は認めなかった. in vitroでのBBLのヒト末梢血リンパ球(PBL)に対するcytotoxicity testでは,96穴マイクロプレートにPBLを1×105cell/wellでtriplicateで分注し,BBLを0〜160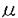 g/mlの濃度勾配でwellに加えて,37℃,5%CO2下で培養し,72時間後に各well中のPBLをtrypan blueで染色して,PBLのviability(%)を求めた.viability(平均±標準偏差)は,BBL濃度0,10,20,40,80,160 g/mlの濃度勾配でwellに加えて,37℃,5%CO2下で培養し,72時間後に各well中のPBLをtrypan blueで染色して,PBLのviability(%)を求めた.viability(平均±標準偏差)は,BBL濃度0,10,20,40,80,160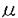 g/mlでそれぞれ98.8±0.9%,97.5±0.3,97.9±2.1%,99.1±0.5%,97.8±0.5%,98.0±0.4%であった.従って,BBLは10〜160 g/mlでそれぞれ98.8±0.9%,97.5±0.3,97.9±2.1%,99.1±0.5%,97.8±0.5%,98.0±0.4%であった.従って,BBLは10〜160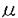 g/mlの濃度でヒトPBLに対する細胞毒性を認めなかった.BBLは200mg/kg/day皮下投与の場合に注射部位の潰瘍形成の副作用はあるが,体内に吸収されれば毒性は非常に少ないと思われた. g/mlの濃度でヒトPBLに対する細胞毒性を認めなかった.BBLは200mg/kg/day皮下投与の場合に注射部位の潰瘍形成の副作用はあるが,体内に吸収されれば毒性は非常に少ないと思われた. 5in vitro,in vivoでのBBLとFKの併用効果の検討 in vitroでは,ヒトPBLのPHA芽球化による3H-thymidine up-takeに対する抑制効果をBBL(10-160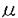 g/ml),FK(0.01〜10nM)の単剤または2剤併用で%inhibitionにより求め,Chou,Kahanのmedian-effect analysisに従って,combination index(CI)を求めることにより,2剤の併用効果を検討した.CIが1未満のとき,併用効果は相乗的と判定した.3名の供血者から得たPBLを用いた検討で,BBL,FKは単剤でともに%inhibitionは濃度依存的に増加した.BBLの50%inhibitionに必要な濃度(Dm値)は34.7〜42.0 g/ml),FK(0.01〜10nM)の単剤または2剤併用で%inhibitionにより求め,Chou,Kahanのmedian-effect analysisに従って,combination index(CI)を求めることにより,2剤の併用効果を検討した.CIが1未満のとき,併用効果は相乗的と判定した.3名の供血者から得たPBLを用いた検討で,BBL,FKは単剤でともに%inhibitionは濃度依存的に増加した.BBLの50%inhibitionに必要な濃度(Dm値)は34.7〜42.0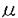 g/mlであった.2剤併用では単剤の場合より%inhibitionは増加し,CI値はBBLとFKのいずれの濃度の組み合わせでも1未満の値を示した.従って,BBLとFKの併用効果は相乗的と判定された(表3). g/mlであった.2剤併用では単剤の場合より%inhibitionは増加し,CI値はBBLとFKのいずれの濃度の組み合わせでも1未満の値を示した.従って,BBLとFKの併用効果は相乗的と判定された(表3).  表3.combination index(供血者1-3のデータから求めたCIの平均値) 表3.combination index(供血者1-3のデータから求めたCIの平均値) 表4.in vivoのデータ(MST)から求めたCI 表4.in vivoのデータ(MST)から求めたCI in vivoでは,実験1で得られたラット肝移植後の平均生存日数(MST)をもとに,MSTから第1群(肝移植後無処置群)の平均生存日数(10.9日を引いた日数を100で除した値をin vitroの場合のfa(%inhibition/100)として,in vitroの場合と同様にCI値を求めて,併用効果を検討した.CI値はMIZとFK0.08mg/kg/day併用の場合,MIZ2.5,5mg/kg/dayでそれぞれ0.48,0.42といずれも1未満の値を示し,MIZとFKの併用効果は相乗的と考えられた.BBL100mg/kg/dayとFK0.08mg/kg/dayの併用の場合もCI値は0.26と1未満の値を示し,BBLとFKの併用効果は相乗的と考えられた. 6.Bリンパ球の抗体産生に対するBBLの抑制効果についての検討 ヌードマウス(BALB/c(nu/nu))にT-cell independent抗原であるDNP-LPS抗原50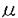 g/bodyを静脈内に投与し,BBL50,100,200mg/kg/dayの腹腔内投与を行って,4日目の血中抗DNP-IgM抗体価をELISA法で測定することによって,BBLのB-cellによる抗体産生能に対する抑制効果を検討した.BBLは200mg/kg/dayの投与量で軽度の抗体産生抑制効果を示した(図3).しかし,MIZや15-deoxyspergualin(DSG)ほどの抑制効果は認めなかった. g/bodyを静脈内に投与し,BBL50,100,200mg/kg/dayの腹腔内投与を行って,4日目の血中抗DNP-IgM抗体価をELISA法で測定することによって,BBLのB-cellによる抗体産生能に対する抑制効果を検討した.BBLは200mg/kg/dayの投与量で軽度の抗体産生抑制効果を示した(図3).しかし,MIZや15-deoxyspergualin(DSG)ほどの抑制効果は認めなかった. 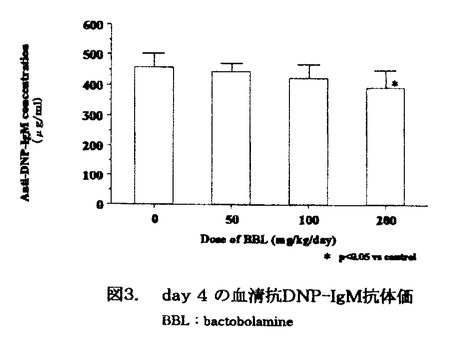 図3. day4の血清抗DNP-IgM抗体価 図3. day4の血清抗DNP-IgM抗体価 |
| 審査要旨 | | 本研究はPseudomonas属に属する細菌株の抗菌性物質bactobolin(BBN)から誘導された微生物二次代謝産物である新しい免疫抑制剤バクトボラミン(BBL)のラット肝移植に対するグラフト生着延長効果,in vivoおよびin vitroにおいてのtacrolimus(FK)との併用効果ならびに副作用について検討したものであり、以下の結果を得ている. 1.ラット肝移植モデル(ACI→LEW)を用いたBBLのグラフト生着延長効果の検討では,肝移植後無処置対照群と比較してBBL50〜200mg/kg/day14日間の皮下投与で用量依存的な生存日数の延長が得られ,BBLとtacrolimus(FK)との併用では,それぞれの単剤投与と比較して有意に(p<0.01)生存日数が延長した.BBLによるグラフト生着延長効果は,単剤投与,FKとの併用投与のいずれもにおいてもmizoribine(MIZ)の効果より優れていた. 2.combination index(CI)を用いたBBLとFKの併用効果の検討では,ヒト末梢血リンパ球(PBL)のPHA(phytohemagglutinin)芽球化に対する抑制をみたin vitroの実験およびin vivo(ラット肝移植)の実験のいずれの場合もその効果は相乗的と考えられた. 3.BBLの薬物動態力学検査では,静脈内投与の場合のAUCを100としたときのBBLのbioavailabilityは,皮下投与,経口投与でそれぞれ25.9%,14.9%であった.AUCの比から求めた投与量(340mg/kg/day)のBBL経口投与では200mg/kg/day皮下投与ほどの効果は得られなかったが,無処置対照群と比較してラット肝移植後の生存日数の有意な延長(p<0.01)が得られた. 4.BBL投与による副作用として200mg/kg/day皮下投与時の皮膚潰瘍を認めたが,340mg/kg/day8日間の経口投与では副作用は認めなかった.ヒトPBLを用いたin vitroでのcytotoxicity testでも,BBLは160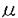 g/ml以下の濃度でヒトPBLに対する細胞毒性を認めなかった. g/ml以下の濃度でヒトPBLに対する細胞毒性を認めなかった. 5.ヌードマウスを用いたBBLの抗体産生能に対する抑制効果の検討では,MIZや15-deoxyspergualin(DSG)ほどの抑制効果は認めなかったが,BBL200mg/kg/day腹腔内投与で有意な(p<0.05)抗体産生の抑制を認めた. 以上,本論文はラット肝移植モデルを用いてBBLの臓器移植後の免疫抑制剤としての有用性を明らかにしたものであり,皮下および経口の単独投与でグラフト生着延長効果を有すること,tacrolimusとの併用で相乗効果を有することを明らかにした.本研究は,従来の薬剤とは全く異なる構造を持つ新しい免疫抑制剤の今後の研究開発に重要な貢献をなすと考えられ,学位の授与に値するものと考えられる. |