根粒菌は、マメ科植物に根粒を形成させ、その中でバクテロイドとなり、共生的窒素固定を行っていることが知られている。根粒形成の初期段階においては、これら2つの生物がつくる分子シグナルの交換が起こることが解明された。根粒菌のそれはNodファクターと名付けられ、このNodファクターがマメ科植物の根に作用し、根粒の形成を引き起こすとされている。 表-1に、今までに分離・同定されたこれらNodファクターの構造を示した。非還元末端部分及び還元末端部分の置換基は、それぞれの根粒菌に特有の修飾が施されており、これによっても、厳格な宿主特異性が決定されている。 この研究において、著者は、アルファルファ菌(R.meliloti)及び大豆菌(B.japonicum)のNodファクターを例にとり、生化学的宿主特異性との関連を調べるために適当な置換基の導入を検討し、各種類縁体及び天然物の合成を検討した。  表-1.各種根粒菌の根粒形成因子(Nodファクター)1.アルファルファ菌の根粒形成因子(Nod Rm-IV(S,C16:2))及びその類縁体の合成 表-1.各種根粒菌の根粒形成因子(Nodファクター)1.アルファルファ菌の根粒形成因子(Nod Rm-IV(S,C16:2))及びその類縁体の合成 Nodファクター合成研究の最初のターゲットとして、表-2に示したようなアルファルファ菌(R.meliloti)の根粒形成因子(Nod Rm-IV(S,C16:2))及びその類縁体を選び検討することとした。  表-2.標的化合物としたNod Rm-IV(S,C16:2)及びその類縁体化合物 表-2.標的化合物としたNod Rm-IV(S,C16:2)及びその類縁体化合物 標的化合物の合成方法は、Scheme1に示したように、まず、グルコサミンの塩酸塩を出発物質とし水酸基を適当な保護基を用いて保護した各単糖部分を合成した。続いて、これら各単糖を順次縮合させ糖鎖の伸長を行い、基本骨格である4糖を得た。最後に、遊離のアミノ基をもつ脱保護体へと変換し、アシル基導入方法を検討し、標的化合物の合成を行った。  ここでのアルファルファ菌の根粒形成因子(Nod Rm-IV(S,C16:2))及びその類縁体の合成の過程では、以下のような知見を得ることができた。 1)まず遊離のアミノ基を有する脱保護体を合成し、合成過程の最終段階でアシル基を導入する合成ルートを開拓することができた。 2)脱保護体にアシル基を導入する方法としては、活性エステル法よりEEDQ法を用いたほうが、効率良くアシル基を導入することができた。 2.大豆菌(USDA135,110,61株)の根粒形成因子(NodBj-V(MeFuc,C18:1))、大豆菌(USDA135株)の根粒形成因子(NodBj-V(MeFuc,C16:0))、大豆菌(USDA61株)の根粒形成因子(NodBj-IV(MeFuc,C18:1))及びその類縁体の合成 次に、Nod Rm-IV(S,C16:2)の合成で得られた知見を利用して、大豆菌の根粒形成因子(NodBj-V(MeFuc,C18:1)、NodBj-V(MeFuc,C16:0)及びNodBj-IV(MeFuc,C18:1))とその類縁体の合成を検討することとした。表-3に、今回、その合成を検討した化合物を示した。  表-3.標的化合物とした大豆菌の根粒形成因子及びその類縁体化合物 表-3.標的化合物とした大豆菌の根粒形成因子及びその類縁体化合物 ここでの大豆菌の根粒形成因子の合成においては、2位にメトキシ基を有するフコース誘導体を、 結合にてグリコシル化を起こさせる際に、3位及4位の水酸基に 結合にてグリコシル化を起こさせる際に、3位及4位の水酸基に -メチルベンゾイル基を保護基として用いると目的物を選択性よく得られることがわかった。 -メチルベンゾイル基を保護基として用いると目的物を選択性よく得られることがわかった。 3.大豆菌(USDA61株)の根粒形成因子(NodBj-IV(Fuc,Gro,C18:1))の合成 今までの一連の根粒形成因子の合成時に得られた知見及び中間体を利用し、大豆菌(USDA61株)のNodファクターを合成することとした。このNodファクターは、グリセロールのC2位の立体配置及び脂肪酸の2重結合の位置等が不明である。そこで、これらのことを明らかにすることを目的として、表-4に示した4つの異性体の合成を行った。 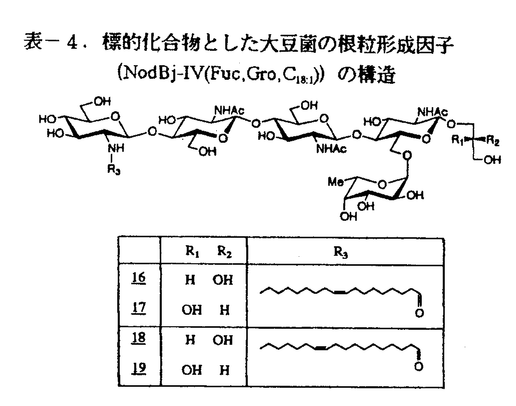 表-4.標的化合物とした大豆菌の根粒形成因子(NodBj-IV(Fuc,Gro,C18:1))の構造 表-4.標的化合物とした大豆菌の根粒形成因子(NodBj-IV(Fuc,Gro,C18:1))の構造 ここでの根粒形成因子(NodBj-IV(Fuc,Gro,C18:1))の合成では、EEDQ法によりアシル基を導入する場合には、還元末端部分がヘミアセタール体の時は反応性が劣るのではないかということが示唆された。 4.生物活性試験 今まで述べてきた一連のNodファクター合成研究で得られたサンプルについて、実際にマメ科植物に対して活性があるかどうかを試験した。 その結果、合成したNodファクター類縁体にも天然物と同様の活性を示すものがあった。また、この生物活性試験の結果より、活性の発現にはアシル基はそれ程重要ではないが、グルコサミン骨格の長さ及び還元末端糖に施される修飾が重要であることが示唆された。 合成の概略は上図の通りである。すなわち既知物質であるグルコサミン誘導体7、24、25、フコース誘導体28、及びグリセロールの両鏡像体を順次結合し、23とした。その後、アシル鎖を最後の段階で導入し、19〜22を合成した。 第四章では、合成したNodファクター類について行った生物試験の結果について論じている。合成したNodファクター類縁体にも天然物と同様の活性を示すものがあり、活性の発現にはアシル基はそれ程重要ではないが、グルコサミン骨格の長さ及び還元末端糖に施される修飾が重要であることがわかった。 以上本論文は、いくつかの、根粒形成因子(Nodファクター)及びその類縁体を合成し、Nodファクター類の合成法を確立するとともに、構造活性相関に関する知見を得たもので、学術上貢献するところが少なくない。よって審査委員一同は、本論文が博士(農学)の学位論文として価値あるものと認めた。 |