腫瘍壊死因子(cachectin/tumor necrosis factor-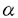 、以下TNF)の臨床応用のための基礎資料となりうる情報を得る目的で、TNFの持続投与により実験動物にみられる栄養学的・生化学的・組織学的な変化を検討した。 、以下TNF)の臨床応用のための基礎資料となりうる情報を得る目的で、TNFの持続投与により実験動物にみられる栄養学的・生化学的・組織学的な変化を検討した。 まずWistar系の雄性ラット(体重約250g)に、致死量以下の比較的大量(1日25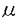 g)のTNFを10日間持続的に静脈内投与し、TNF群とした。TNF群におけるさまざまなパラメーターの変化を、生食群(生理食塩水を静脈内投与し食餌を自由に摂取させた群)と、PF群(生理食塩水を静脈内投与しTNF群の各ラットと毎日同量の食餌を与えた群=pair-fed群)を対照群として、比較検討した。 g)のTNFを10日間持続的に静脈内投与し、TNF群とした。TNF群におけるさまざまなパラメーターの変化を、生食群(生理食塩水を静脈内投与し食餌を自由に摂取させた群)と、PF群(生理食塩水を静脈内投与しTNF群の各ラットと毎日同量の食餌を与えた群=pair-fed群)を対照群として、比較検討した。 実験動物においてTNFの投与によりみられる食餌摂取量の低下に関して、従来その機序は知られていなかったが、TNF群では脳内の生体アミンおよびその関連物質のうちで、セロトニンの前駆物質のトリプトファンと代謝産物の5-HIAAの濃度が生食群やPF群よりも高く、脳内のセロトニンの増加と食餌摂取量の低下の因果関係が示唆された(図1)。なおドパミン・ノルアドレナリン・ホモバニリン酸(HVA)・ジヒドロキシフェニル酢酸(DOPAC)の脳内の濃度には、各群間で有意差はなかった。このことから、TNFが関与すると考えられる悪性腫瘍や感染症などの病態において、セロトニンの動態あるいは作用を修飾することにより患者の食物摂取量を増加させる可能性が考えられる。たとえばセロトニン受容体拮抗薬の有用性の検討、あるいは栄養療法として、セロトニンの前駆物質であるトリプトファンを除去した食物や、トリプトファンの脳内への移行を抑制する分枝鎖アミノ酸に富む食物の投与の検討である。 組織の生化学的検討では、筋肉(長趾伸筋・横隔膜)中の蛋白量・DNA量は、TNF群とPF群で差はなかったが、両群とも生食群よりも少なかった。TNF群では、肝の蛋白量はPF群よりも多く、肺の蛋白量は生食群およびPF群よりも多かった。またTNF群では、肝・肺・心におけるDNA量は生食群およびPF群よりも多かった(図2)。 組織学的検討で以下の所見は、TNF群のみに認められ、生食群およびPF群では認めなかった。すなわち(1)肝におけるグリソン鞘を中心とする肝細胞の脱落、偽胆管様構造を形成する細胞の増生、および肝細胞の分裂像、(2)心における心内膜下の繊維芽細胞様細胞の増生、およびその心筋細胞への浸潤、(3)肺における肺胞中隔の肥厚、および肺胞マクロファージの増加、(4)肝と脾における髄外造血、(5)肝と肺の静脈内における白血球の鬱滞、および静脈内での単球/マクロファージによる赤血球貪食、である。 血液生化学的には、TNF群のみにヘマトクリット値の低下とBUNの上昇を認め、TNF群ではPF群にみられた低血糖を認めなかった。 TNFの持続投与10日目の安静時代謝率およびエネルギー消費量は、TNF群の方がPF群より有意に大きかった(図3)。 次にWistar系の雄性ラット(体重約250g)を対象に、TNFを浸透圧ポンプにより、1日15 g2日間持続的に腹腔内投与し、肝におけるKupffer細胞の活性化の有無、肺における組織の変化とヒドロキシプロリンの増加の有無、末梢血中の脂質過酸化物の増加の有無を検討した。 g2日間持続的に腹腔内投与し、肝におけるKupffer細胞の活性化の有無、肺における組織の変化とヒドロキシプロリンの増加の有無、末梢血中の脂質過酸化物の増加の有無を検討した。 摘出肝標本をnitro blue tetrazoliumおよびphorbol myristate acetateで還流することによって、TNF群においては肝内のKupffer細胞/マクロファージ中のsuperoxide anion産生亢進によるformazan顆粒の著明な増加、すなわちKupffer細胞/マクロファージが活性化していることが示された。 TNF投与2日後に、摘出肺では蛋白量は増加していたが、ヒドロキシプロリン量は増加せず、肺内には非コラーゲン性蛋白が増加していると考えられた。肺組織では肺胞中隔の肥厚と肺胞内のマクロファージの増加を認めた。 TNF投与2日後では、TNF群での血中の脂質過酸化物の増加は認めなかった。 これらの結果は、TNFの持続投与により生体にみられるさまざまな変化のうち、筋肉蛋白の減少は単純な飢餓の場合と同様であるが、以下のようなさまざまな変化は単純な飢餓の場合とは異なることを示している。すなわち(1)脳内のセロトニン関連物質の増加と比較的な高血糖を伴う食餌摂取量の減少、(2)肝・肺・心における蛋白・DNAの増加、(3)肝・心における細胞の増生、(4)肝・肺におけるマクロファージの活性化、(5)貧血、および血液中での単球/マクロファージによる赤血球貪食、(6)骨髄の過形成と肝や脾における髄外造血、(7)肝や肺の静脈内での白血球の鬱滞、(8)安静時の代謝率とエネルギー消費量の増加、などである。 本研究においては、TNFそのものを実験動物にin vivoで長期間持続的に投与して、実験動物にみられる変化を検討したため、TNFのみの作用ではなく二次的に産生されたその他のサイトカインの作用も加わっている可能性がある。しかし将来TNFの特定の作用を強化あるいは抑制するための方法を考えていくためにも、またTNFのもつ多彩な作用のうちで特定の作用のみを有し他の作用をもたないmodified TNFを遺伝子工学的に開発していくためにも、このような検討が必要であると思われる。  (図1) (図1) (図2) (図2) (図3) (図3) |