1929年にA.Flemingがブドウ球菌の生育が強く阻害されていることを発見し、その活性物質をペニシリンと命名して以来、多くの有用な抗生物質が天然界より得られている。しかし、これまでのどのような抗生物質に対しても、時間の経過とともに耐性を獲得した病原菌が出現していることから、常に新しい抗生物質が求められている。現在でも、特にMRSA(Methicillin Resistant Staphylococcus Aureusメチシリン耐性黄色ブドウ球菌)及び緑膿菌に対し有効な抗生物質の開発が望まれている。 著者は、新規な骨格を有する抗生物質の発見を目標として、土壌から分離した微生物の生産物をスクリーニングしてきた。このなかから、Micrococcus luteusに対し抗菌活性を示す化合物を生産する放線菌を、東京都品川区の微生物化学研究所の敷地内の土壌より分離した。この放線菌をMI178-34F18と命名し、その培養液から新規な7種の化合物を単離しパイラロミシン1a〜1d(1〜4)、2a〜2c(5〜7)と命名した(Fig.1)。パイラロミシン群はクロモフォアとしてベンゾピラノピロールを有し、1〜4ではサイクリトールが、5〜7では糖がクロモフォアの窒素原子に結合している。ベンゾピラノピロールは既に抗生物質TAN-876Aの基本骨格として報告されているが、その窒素原子がアルキル化された化合物として、パイラロミシン群が初めての物質である。また、サイクリトールを置換基として持つアナログと、糖を置換基として持つアナログとが同時に生産されることも興味深い。  Fig.1.Structures of pyralomicins 1a,1b,1c,1d,2a,2b and 2c. Fig.1.Structures of pyralomicins 1a,1b,1c,1d,2a,2b and 2c. 本論文ではパイラロミシン群物質の生産菌の同定、パイラロミシン群物質の単離精製、構造決定、生合成及び生物活性について記述し、以下にその概略を述べる。 第1章では、パイラロミシン群物質の生産菌の同定、生産、及び精製について述べる。パイラロミシン群抗生物質の生産菌はその培養性状、生理学的性質、細胞壁の構成成分からMicrotetraspora属と決定し、性状の類似する2種類の菌株(Microtetraspora spiralis及びMicrotetraspora salmonea)を選抜して、比較試験を行った。その結果、本菌株をMicrotetraspora spiralis MI178-34F18とした。この菌株を培養タンクによって114時間通気培養した後、培養液上澄から溶媒抽出、シリカゲルカラムクロマトグラフィー、逆相高速液体クロマトグラフィーを用いてパイラロミシン群の7種の化合物を精製した。 第2章では、パイラロミシン群物質の理化学的性状について述べ、引き続きNMRスペクトルの解析に基づくパイラロミシン群物質の構造決定について述べる。パイラロミシン群の7種類の物質は、それらの理化学的性状の類似性から共通のクロモフォアを有することが示唆された。構造決定は、まず、最も収量の多かったパイラロミシ1a(1)について行い、その結果に基づいて、2〜7の構造を検討した。この構造研究において、1H-NMR、13C-NMR、1H-1HCOSY、HMQC及び1H-13CHMBC以外に、1H-15N HMBC及び1Hを選択的に照射した13C NOE差スペクトルを用いて解析を行った。この2つのNMR実験法は水素原子の少ないパイラロミシン群のクロモフォア部分の構造決定において、非常に有効であった。これらの解析の結果、パイラロミシン1a(1)はベンゾピラノピロールをクロモフォアとし、ピロール環の窒素原子を介してサイクリトールを持つ、ユニークな構造を有することを明らかにした。パイラロミシン1b〜1d(2〜4)は1と同様にピロール環の窒素原子を介してサイクリトールを有していたが、パイラロミシン2a〜2c(5〜7)はサイクリトールにかわり、グルコピラノースを有していた。パイラロミシン群の代表的な化合物であるパイラロミシン1a(1)及び2a(5)については1H-1Hスピン結合定数の解析及び、それぞれのアセチル誘導体を用いた差NOE実験により相対立体構造の解析を行った。さらに、パイラロミシン1a(1)及び2a(5)のp-ブロモベンゾイル誘導体を用いて、それぞれX線結晶解析を行い、臭素原子の異常分散効果により絶対立体配置を決定した。その結果1は2,6-dichloro-1-[(1R,4R,5S,6S)-5,6-dihydroxy-3-(hydroxymethyl)-4-m eth oxy-2-cyclohexen-1-yl]-5-hydroxy-8-methyl-[1]benzopyrano[2,3-b]pyrrole-4-(1H)-oneであり、5は2,6-dichloro-5-hydroxy-8-methyl-1-(4-O-methyl-b-D-glucopyranosyl)-[1]benzopyrano[2,3-b]pyrrole-4(1H)-oneであると決定した。2〜4及び6〜7の絶対構造はそれらのCDスペクトルを1及び5のCDスペクトルと比較して決定した。 第3章では、パイラロミシン群物質の生合成について述べる。生合成研究は最も生産量の多いパイラロミシン1a(1)について行った。パイラロミシン群抗生物質生産菌の培養液中に、各種の13C標識化合物を添加し、取り込まれた13C標識の位置を13C-NMRを用いて調べる方法で炭素原子の由来を調べ、また、15N標識化合物を用いる取り込み実験を行い15N-NMRを用いて窒素原子の由来を調べた結果、パイラロミシンのクロモフォア部分は2分子の酢酸、1分子のプロピオン酸、1分子のプロリンを前駆体として生合成されることを明らかにした。この生合成研究において特に興味深いことは、クロモフォア部分のピロール環がプロリンに由来し、また、このピロール環に結合するカルボニル基が、転位したプロリンのカルボキシル基に由来すると推測されたことである(Fig.2)。パイラロミシン1a(1)のサイクリトール部分はグルコースに由来するC2、C2、C3のユニットより構成されることから、ペントース・リン酸経路を経て生合成されると推定した(Fig.2)。パイラロミシン2a(5)のグルコピラノース部分はグルコースに由来するが、直接取り込まれたものではなく、またその再構成の経路も複数存在することが示された。この経路は解糖系・糖新生経路及びペントース・リン酸経路を経由するものと推定した。 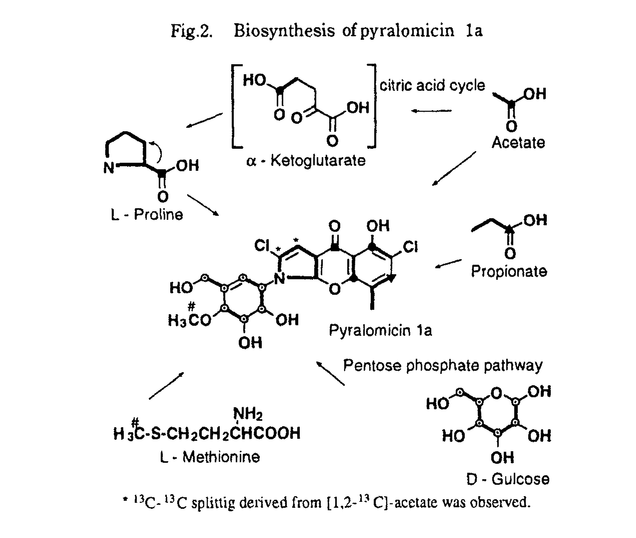 Fig.2.Biosynthesis of pyralomicin 1a Fig.2.Biosynthesis of pyralomicin 1a 第4章では、パイラロミシン群の生物活性について述べる。パイラロミシン群はMicrococcus luteusに対し各成分により異なる抗菌活性を示し、その濃度範囲は0.2〜25mg/mlであった。Escherichia coli BE1121及びE.coli BE1186に対しパイラロミシン群の各成分は1.56〜100mg/mlの濃度範囲で抗菌活性を示した。しかし、その他の細菌あるいは真菌に対しては、殆ど活性を示さなかった。また、パイラロミシン1a(1)と2a(5)の混合物はマウス腫瘍細胞に対し、in vivoで抗腫瘍活性を示した。パイラロミシン群は培養腫瘍細胞に対し、細胞毒性はIC50が10mg/ml以上であった。パイラロミシン1a(1)及び2a(5)はいずれもマウスに対し100mg/kgで毒性を示さなかった。 |