細胞周期とは細胞の増殖過程で1個の母細胞が2個の娘細胞に分裂する一連のプロセスのことで、通常、分裂期(M期)、DNA合成準備期(G1期)、DNA合成期(S期)と分裂準備期(G2期)に大別される。細胞周期の制御機構の解明は、生命現象の謎を探るバイオサイエンスの重要な課題の一つであり、また、細胞の無秩序な異常増殖である癌の克服にも大いに寄与することと期待されている。細胞周期制御機構の解明において低分子阻害剤の開発と応用は分子生化学的手法として利用され注目を浴びている。一方、現在臨床使用中または開発中の抗癌剤には、ビンカアルカロイドやタキソールのように染色体分配を阻害して細胞周期をM期で停止させる作用を示すもの、5-フルオロウラシルやサイクロホスファミドのようにDNA合成を阻害してS期に停止させる作用を示すものなど、それらが必ずしも細胞周期に対する制御活性を意識して開発されたわけではないにも関わらず、細胞周期に特徴的な阻害作用を示すものが多い。従って、新しい細胞周期阻害剤は細胞機能解析のためのツールとしてだけでなく新抗癌剤としての展開が期待される。 本研究ではマウス乳癌tsFT210細胞を用いて微生物代謝産物より新規細胞周期阻害剤の探索を行った。陸上および海底土壌由来の微生物数千株の培養物について細胞周期阻害活性を調べた結果、静岡県大井川沖海底の土壌より分離した糸状菌Aspergillus fumigatus BM939株が新規阻害剤を生産することを見出した。更に、その培養物より活性成分を追求し、新規骨格のspirotryprostatin A(1)、B(2)、新化合物のtryprostatin A(3)、B(4)とcyclotrypro-statin B(8)、D(10)、また、新天然物としてcyclotryprostatin A(7)、C(9)とdemethoxyfumitre-morgin C(5)および既知化合物のfumitremorgin C(6)など一連のdiketopiperazine類化合物(Chart 1)を、細胞周期の新しいG2/M期阻害剤として単離し構造決定した。 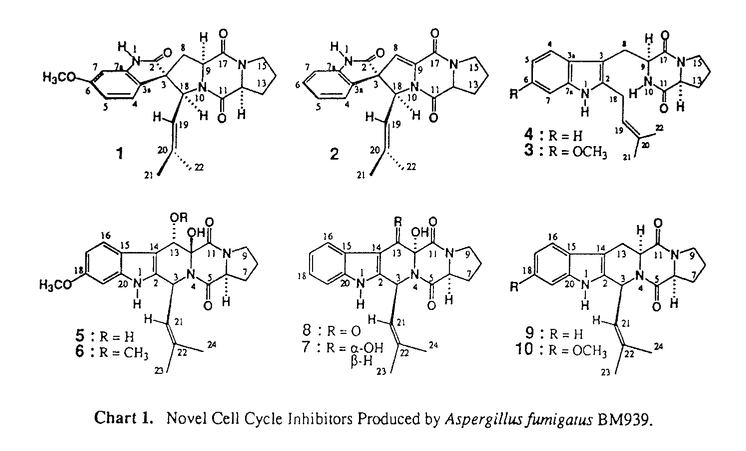 Chart 1. Novel Cell Inhibitors Produced by Aspergillus fumigatus BM939. Chart 1. Novel Cell Inhibitors Produced by Aspergillus fumigatus BM939. 本論文は上記天然diketopiperazine類新規細胞周期阻害剤の単離精製、構造解析並びに生物活性についてまとめたものである。 1.新規細胞周期阻害剤の醗酵生産および単離精製 前記生産菌株を、グルコース3%、可溶性澱粉2%、大豆粉2%、リン酸水素二カリウム0.5%、および硫酸マグネシウム0.05%を含む培地100ml(pH6.5)に接種し、28℃で47時間振盪培養した後、同組成の培地18Lを有する30Lジャーファメンターに移して28℃で24時間種培養(毎分350回転、毎分9Lの通気)を行った。この種培養液を、同組成の培地400Lに加え、600Lジャーファメンターにて28℃で66時間にわたって生産培養(毎分350回転、毎分200Lの通気)を行い、計410Lの培養液を得た。 上記培養液を吸引ろ過して菌体と上清(370L)に分離し、上清を400Lの酢酸エチルで1回抽出した。菌体は90%アセトン400Lで抽出し、減圧濃縮して得られる水溶液(60L)を酢酸エチルで抽出した(120Lx2回)。全酢酸エチルを濃縮し、褐色のシロップ1.2Lを得た。 このシロップを繰り返し溶媒抽出や液体分配およびシリカゲルカラムクロマト、中圧液体クロマト、HPLCなどの組み合わせにより分離精製した結果、化合物1、2、3、4、5、6、7、8、9、10をそれぞれ1.2mg、11mg、 1048mg、64.4mg、159.6mg、903.5mg、1.0mg、4.4mg、12.4mg、1.2mgずつ得ることができた。 2.新規細胞周期阻害剤の構造研究 Spirotryprostatin A、Bの構造:Spirotryprostatin A(1)、B(2)の分子式はそれぞれC22H25N3O4(1)、C21H21N3O3(2)と決定され、UVとIR吸収により芳香環やdiketopiperazine骨格の存在が推測された。次に、1H-1H COSY、PFG-HMQCや差NOE実験結果より、プロトンスピン系による部分構造を導き、部分構造間のつながりをPFG-HMBCスペクトルの解析により明らかにして平面構造を決定した。相対立体構造はNOE差スペクトルの解析結果をもとに、また、絶対構造は酸加水分解結果およびCDスペクトルにより決定した。 Spirotryprostatin A(1)、B(2)は、ベンゼン環と縮合した5員環ラクタムおよびジケトピペラジンと縮合したヘテロ5員環から形成されたスピロ骨格を有するユニークな新規骨格の化合物で、その構造は1個のトリプトファン単位、1個のプロリン残基および1個のイソプレニル基より形成されており、トリプトファン単位はすでに1、2においてC2/C3位の水素化とC2位の酸化または2においてC8/C9位の更なる脱水素化などの修飾を受けている。今まで、トリプトファンとプロリンから形成されたdiketopiperazine類スピロ化合物が自然界より発見された例は数少なく、すべての既知化合物が1、2とは異なるスピロ環骨格を有している。また、2個のヘテロ5員環よりスピロ骨格を形成した化合物としてはtryptoquivaline類が知られているが、いずれも構造は全く異なる。本化合物のような骨格をなすものは先例がなく、今回、新規骨格構造の1、2を新しい細胞周期阻害剤として初めて天然から発見した。 Tryprostatin A、Bの構造:Tryprostatin A(3)、B(4)はそれぞれ分子式C22H27N3O3とC21H25N3O2の化合物で、特徴的なUV吸収パターンより3に6-O-methylindole chromophoreの存在が、4にはindole chromophoreの存在が示唆された。また、IR吸収より両者にdiketopiperazine骨格の存在が示唆された。1H-1H COSY、PFG-HMQCや差NOE実験結果よりプロトンスピン系による部分構造を、さらにPFG-HMBCにより部分構造の連結を明らかにし平面構造を決定した。相対立体構造はNOE結果より、絶対構造は[ ]DとCDデータをもとに決定した。 ]DとCDデータをもとに決定した。 Tryprostatin A(3)、B(4)は、2-イソプレニルトリプトファンとプロリン残基から形成されたdiketopiperazine構造を有する化合物で、同種カビの代謝産物より単離されたverruculogenやfumitremorgin類と比べ、18位と10位間のC-N結合が切断され、中心部のヘテロ環構造が開環されている点で非常にユニークな化合物である。Tryprostatin A(3)、B(4)と構造的に類似した天然物としてはdeoxybrevianamide-Eが知られているが、この化合物は2位における置換基が異なり、その生物活性に関する報告もみられなかった。 Fumitremorgin類5,6およびCyclotryprostatin A-D(7-10)の構造:これらの化合物の分子式はいずれも3個の窒素を含有し、特徴的なUV吸収パターンより6、7と8に6-O-methylindole chromophoreの存在が、また、5と9にはindole chromophoreの存在が示唆され、10にはさらに伸びた共役系chromophoreの存在が示唆された。いずれの化合物においてもIR吸収よりdiketopiperazine骨格の存在が推測されたが、10ではさらに共役したカルボニル吸収が認められた。次に、1H-1H COSY、PFG-HMQCや差NOE実験結果より各々のプロトンスピン系による部分構造を導き、PFG-HMBCにより部分構造を繋ぎ合わせ平面構造を決定した。相対立体構造はNOEなどNMRデータにより、絶対構造は酸加水分解結果とCDにより決定した。 以上の結果、6は同属菌に生産される既知化合物のfumitremorgin Cと同定した。化合物5と7-10はいずれも新しい天然diketopiperazine類であるが、5、7と9はfumitremorgin類の合成過程で既に合成された化合物で、今回初めて天然品として単離された。また、化合物7-10はいずれもfumitremorgin類と同様な骨格をもつが、10の場合13位がケトンに酸化されているのが特徴的で新化合物であり、7と8は12S配置を有する天然物として最初の例で生合成的に興味の持たれる重要な化合物である。これらの化合物はtryprostatinと化学構造および生物活性上の類似性よりそれぞれcyclotryprostatins A(7),B(8),C(9),D(10)と命名した。 一方、上記化合物の絶対構造の研究過程で、CD Cotton効果と絶対構造との関連性に関する有益な知見が得られた。これらは類縁化合物の絶対構造研究に有用な手法を提供するものと思われる。 3.新規細胞周期阻害剤の生物活性 細胞周期阻害活性は、細胞周期のG2/M期進行に必須であるcdc2キナーゼが温度感受性に変異したマウスtsFT210細胞を用い、細胞核をPropidium Iodideにより染色後、フローサイトメトリーにて測定した。化合物1-10はいずれも細胞周期阻害活性を示し、数 M〜数十 M〜数十 Mの濃度域でtsFT210細胞の細胞周期をG2/M期に停止させた。IC50値はそれぞれ197.5 Mの濃度域でtsFT210細胞の細胞周期をG2/M期に停止させた。IC50値はそれぞれ197.5 M(1),14.0 M(1),14.0 M(2),78.7 M(2),78.7 M(3),18.8 M(3),18.8 M(4),1.78 M(4),1.78 M(5),14.0 M(5),14.0 M(6),5.6 M(6),5.6 M(7),19.5 M(7),19.5 M(8),23.4 M(8),23.4 M(9),25.3 M(9),25.3 M(10)であり、構造-活性相関に関する有益な知見も得られた。また、染色体の蛍光染色法による形態学的観察結果により、l、2、7-10が細胞周期をG2およびM期の2カ所で停止させるのに対し、3-6は主にM期で阻止することを明らかにした。 M(10)であり、構造-活性相関に関する有益な知見も得られた。また、染色体の蛍光染色法による形態学的観察結果により、l、2、7-10が細胞周期をG2およびM期の2カ所で停止させるのに対し、3-6は主にM期で阻止することを明らかにした。 化合物1-10はいずれもcdc2キナーゼ活性を直接阻害せず、さらに、PKA、PKC、EGF-Rなどの蛋白質リン酸化酵素に対する阻害作用も示さなかった。一方、1-4の微小管重合に対する作用を調べた結果、いずれにもin situおよびin vitroにおける微小管重合阻害活性が認められた。これらの結果および染色体の形態学的特徴より、1-10が直接分裂装置に作用することが示唆された。 結論: 上記本研究の成果により、新規骨格のspirotryprostatin等の新規細胞周期阻害剤が提供された。これらの阻害剤には、構造の新規性や生物活性等より、今後作用機構の解明と生物学的研究の進展に伴って低分子プローブや新抗癌剤としての展開が期待される。 |