アトピー性疾患の原因となるIgEの産生においては、タイプIIのヘルパーT(Th2)細胞とB細胞の間の相互作用を介して、免疫グロブリンのクラススイッチが誘導される。まず、抗原がB細胞表面の免疫グロブリンを介して取り込まれると、プロセスされた後、MHC(主要組織適合抗原)クラスII分子によって提示される。これを認識して活性化されたTh2細胞はインターロイキン4(IL-4)を産生し、その作用によりB細胞はgermline IgE mRNAを発現する。このmRNAはタンパクに翻訳されないが、その発現は次のクラススイッチの誘導に不可欠であることが明らかにされている。そして、活性化Th2細胞が発現するCD40リガンドがCD40と結合することによりB細胞に第二の刺激が伝わると、免疫グロブリン遺伝子定常領域間のスイッチ領域を介して遺伝子組換え(クラススイッチ)が起こり、成熟型IgE mRNAが発現してIgEが産生される。このように、IL-4はB細胞に作用してIgEへのクラススイッチを誘導するが、同時にIL-4レセプター(IL-4R)の発現を増強することが知られている。自らのレセプターを発現増強するサイトカインは他には少なく、IL-4にユニークな作用であるが、その意義については不明である。本研究では、IL-4Rの発現増強がIgE産生誘導においても何らかの役割を担っているのではないかという観点から検討を加えるとともに、アトピー患者のリンパ球を用いてIL-4Rの発現レベルを解析した。また、IgE産生の誘導に必要なシグナル伝達分子のひとつとして、protein kinase C(PKC)の関与について検討を行った。 まず、IL-4刺激によるIL-4Rの発現増強を確認するため、ヒト扁桃由来B細胞をIL-4存在下で48時間培養した結果、Kd=81nMの高親和性結合部位が細胞当たり約300個存在し、IL-4はその数を約2倍に増加させた。IL-4RはIL-4R 鎖とcommon 鎖とcommon  ( ( c)鎖(IL-2R/IL-7R/IL-9R/IL-15Rと共通のサブユニット)とから構成されるが、IL-4R c)鎖(IL-2R/IL-7R/IL-9R/IL-15Rと共通のサブユニット)とから構成されるが、IL-4R 鎖mRNAの発現増強が確認されたのに加え、 鎖mRNAの発現増強が確認されたのに加え、 c鎖mRNAも発現増強されることが見いだされた。末梢B細胞を用いてIL-4R発現増強のIL-4濃度依存性を調べると、20U/mlで有意に増加したのに対し、末梢血単核細胞(PBMC)をIL-4で刺激するIgE産生誘導系では、100U/mlのIL-4でも産生されるIgE量はわずかであり、両活性の間でIL-4に対する感受性に差がみられた。 c鎖mRNAも発現増強されることが見いだされた。末梢B細胞を用いてIL-4R発現増強のIL-4濃度依存性を調べると、20U/mlで有意に増加したのに対し、末梢血単核細胞(PBMC)をIL-4で刺激するIgE産生誘導系では、100U/mlのIL-4でも産生されるIgE量はわずかであり、両活性の間でIL-4に対する感受性に差がみられた。 発現増強されたIL-4RがIgE産生誘導の過程で果たす役割を検討する手段として、IL-4R cDNAの翻訳開始部位付近の配列に対するアンチセンスDNA(S-oligo 1;5-GAGCCCAGAGCAAAGCCACCCCAT-3)を合成した。その効果を、IL-4Rの発現レベルが高いDaudi細胞(500個/細胞)の培養液中に加えて比較したところ、IL-4Rの発現を強く抑制した。S-oligo 1の作用は末梢B細胞でも確認され、S-oligo 1 5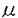 MをIL-4刺激と同時に添加すると、IL-4Rの発現増強は約50%抑制された。また、IL-4はIL-4RだけでなくCD23・CD40・HLA-DR・IgMの発現を増強することが知られているが、S-oligo 1はこれらの分子の発現には影響しないことから、その作用の特異性が確認された。そこで、IL-4と抗CD40抗体を用いたT細胞非依存的なIgE産生誘導系にS-oligo 1を添加したところ、IgE産生量が濃度依存的に抑制されるのに対し、IgG産生量に影響はなかった(図1)。 MをIL-4刺激と同時に添加すると、IL-4Rの発現増強は約50%抑制された。また、IL-4はIL-4RだけでなくCD23・CD40・HLA-DR・IgMの発現を増強することが知られているが、S-oligo 1はこれらの分子の発現には影響しないことから、その作用の特異性が確認された。そこで、IL-4と抗CD40抗体を用いたT細胞非依存的なIgE産生誘導系にS-oligo 1を添加したところ、IgE産生量が濃度依存的に抑制されるのに対し、IgG産生量に影響はなかった(図1)。  図1 IL-4Rに対するアンチセンスDNA(S-oligo 1)のIgE産生に及ぼす効果ヒトB細胞をS-oligo 1の存在下でIL-4と抗CD40抗体により14日間刺激した。(mean±SE,n=3) 図1 IL-4Rに対するアンチセンスDNA(S-oligo 1)のIgE産生に及ぼす効果ヒトB細胞をS-oligo 1の存在下でIL-4と抗CD40抗体により14日間刺激した。(mean±SE,n=3) S-oligo1のIgE産生抑制作用をmRNAレベルで解析したところ、germline IgE mRNAの発現レベルにほとんど変化はみられず、mature IgE mRNAの発現のみが抑制されていたことから、発現増強されたIL-4Rはクラススイッチの誘導を促進していることが示唆される。その機序としては、1)クラススイッチを誘導するシグナルの閾値がgermline IgE mRNAの発現の閾値に比べて高く、レセプター数の増加が必要であるという可能性や、2)新たに発現したレセプターが既存のレセプターとは異なるシグナル伝達機構と会合する可能性が考えられる。 一方、IFN- はIgE産生を含むIL-4の生物活性の多くに対して拮抗作用を示すことが知られているが、IL-4Rの発現増強には影響しなかった。従って、IFN- はIgE産生を含むIL-4の生物活性の多くに対して拮抗作用を示すことが知られているが、IL-4Rの発現増強には影響しなかった。従って、IFN- はIL-4R発現増強以降のステップでIgE産生を抑制することが明らかになった。 はIL-4R発現増強以降のステップでIgE産生を抑制することが明らかになった。 次に、IL-4Rの発現増強が生体内でも誘導されることを検出するために、IgE産生が亢進しているアトピー患者のリンパ球に発現しているIL-4Rを解析した。末梢血より分離直後のB細胞では、健常者と患者の間でIL-4Rの数や親和性に差はみられなかった。そこで、分離後のリンパ球を37℃2時間インキュベートしてから125I-IL-4結合量を測定したところ、患者リンパ球ではインキュベート前に比べて結合量が増加した。この増加は、生体内ですでにIL-4Rに結合していた内因性IL-4が解離したことによるものと考えられる。また、分離した患者リンパ球をIL-4存在下で48時間培養した場合、健常者リンパ球とは異なり、IL-4Rの発現増強が全く誘導されない例が多数を占めた。これらの結果は、アトピー患者の体内では、内因性IL-4によりリンパ球上IL-4Rの発現がmaximumに亢進していることを示している。 IL-4のシグナル伝達機構に関してPKCの関与を示唆する報告があるが、IgE産生誘導におけるPKCの必要性については明らかでない。そこで、IL-4に応答してgermline IgE mRNAを発現するヒトBurkitt lymphoma B細胞株であるDND39を用いて検討を行った。まず、PMAがIL-4によるgermline IgE mRNAの発現を増強することが確認され、またPKC阻害剤のひとつであるK252bがgermline IgE mRNAの発現を抑制することからPKCの関与が強く示唆された。さらに、PKCの活性化に関与するsecond messengerを測定したところ、diacylglycerolやIP3の上昇が確認されたが、Ca2+レベルの上昇はみられなかった。また、IL-4によるphosphatidylinositol3-kinase(PI3-kinase)の活性化が他の細胞種で報告されているが、B細胞でもPI3-Pの生成が検出され、PI3-kinaseの活性化が確認された。 そこで、Ca2+非依存性のPKC isozymeに関してIL-4刺激によるtranslocationを解析したところ、PKC および および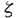 のtranslocationが認められ、これらがgermline IgE mRNAの発現に関与する可能性が考えられた。PKC のtranslocationが認められ、これらがgermline IgE mRNAの発現に関与する可能性が考えられた。PKC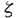 は、ATP結合領域のC末端に位置するLysをTrpに置換すると、dominant negativeに作用することが報告されているので、そのようなmutant PKC は、ATP結合領域のC末端に位置するLysをTrpに置換すると、dominant negativeに作用することが報告されているので、そのようなmutant PKC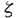 の発現プラスミドを構築し、レポータープラスミド(ルシフェラーゼ遺伝子の上流にgermline IgE遺伝子のプロモーター領域をつなげたもの)と共に細胞に導入した後、IL-4刺激で誘導されるルシフェラーゼ活性を測定した。その結果、wild type PKC の発現プラスミドを構築し、レポータープラスミド(ルシフェラーゼ遺伝子の上流にgermline IgE遺伝子のプロモーター領域をつなげたもの)と共に細胞に導入した後、IL-4刺激で誘導されるルシフェラーゼ活性を測定した。その結果、wild type PKC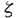 を導入した場合に比べ、mutant PKC を導入した場合に比べ、mutant PKC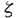 を導入した場合には、IL-4に対する反応性が約50%抑制されており、PKC を導入した場合には、IL-4に対する反応性が約50%抑制されており、PKC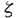 がgermline IgE mRNAの発現に関与することが明らかになった。ただし、PKC がgermline IgE mRNAの発現に関与することが明らかになった。ただし、PKC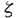 はPMA非応答性であることから、PMAによるgermline IgE mRNAの発現増強には他のPKC isozymeも関与している可能性は残されている。 はPMA非応答性であることから、PMAによるgermline IgE mRNAの発現増強には他のPKC isozymeも関与している可能性は残されている。 以上を総括すると 1)IL-4によるIgE産生誘導の過程では、まずIL-4Rの発現が増強され、発現増強したIL-4Rがクラススイッチの誘導を促進する。 2)IgE産生が亢進しているアトピー患者の多くでは、リンパ球上のIL-4Rが実際に発現亢進している。 3)IL-4によるgermline IgE mRNAの発現にはPKC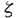 が関与している。 が関与している。 |