| 内容要旨 | | 近年の有機合成化学の急速な発展に伴い、綿密な合成計画のもとで種々の合成手段および測定手段を駆使すれば極めて複雑な構造を持つ化合物も合成できるという考えが、現在では通念になっている。しかし、一方で発見以来多くの年数が経つにもかかわらず、未だに合成が困難な化合物も多数存在している。これら化合物を合成するためには、合成手法となる優れた分子変換反応の開発が必要となる。すなわち、穏やかな条件下で選択的にしかも効率良く進行する分子変換法の開発は、現在の有機合成化学の重要な研究課題となっている。とくに、医薬・農薬・香料に代表される生理活性を示す化合物は光学活性である場合が多く、これらの合成にあたっては、望みの光学活性体だけを選択的に合成する不斉合成法の開発も強く求められている。 著者はまず二価スズトリフラート-光学活性ジアミン-四価スズ化合物の組合せからなる複合系不斉触媒を用いる不斉アルドール反応を活用して、種々の光学活性1,2-ジオール類を高立体選択的に合成する手法を開発した。さらにこの反応を活用して次世代の有望な抗癌剤として期待される微量天然化合物タキソールの不斉全合成を達成した。以上の研究結果について、2章にわたって述べる。 1.二価スズトリフラート-光学活性ジアミン錯体を用いる不斉アルドール反応 二価スズトリフラート-光学活性ジアミン錯体-四価スズ化合物を不斉触媒に用いると、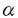 -ベンジルオキシチオ酢酸エステル由来のシリルエノールエーテルとアルデヒドから、ほぼ完全なジアステレオ及びエナンチオ選択性でアンチ立体配置を有する光学活性な -ベンジルオキシチオ酢酸エステル由来のシリルエノールエーテルとアルデヒドから、ほぼ完全なジアステレオ及びエナンチオ選択性でアンチ立体配置を有する光学活性な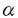 、 、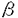 -ジヒドロキシエステル等価体が得られることを見い出した(第一章・第二節)。次に、上記の反応の遷移状態の考察から、チオ酢酸エステルの -ジヒドロキシエステル等価体が得られることを見い出した(第一章・第二節)。次に、上記の反応の遷移状態の考察から、チオ酢酸エステルの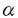 位の置換基をかさ高いt-ブチルジメチルシロキシ基に変えれば逆のジアステレオマーが生成するのではないかと考えた。事実、この方法でシン立体配置を有する光学活性 位の置換基をかさ高いt-ブチルジメチルシロキシ基に変えれば逆のジアステレオマーが生成するのではないかと考えた。事実、この方法でシン立体配置を有する光学活性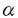 、 、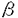 -ジヒドロキシエステル等価体が合成できることを明らかにした。以上、チオ酢酸エステルの -ジヒドロキシエステル等価体が合成できることを明らかにした。以上、チオ酢酸エステルの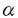 位水酸基の保護基を選択するだけで望みの立体配置を持つ光学活性1,2-ジオールを合成できる、簡便な方法を確立した(第一章・第四節)。従来オレフィン類の不斉酸化法しか良い合成法の知られていない光学活性1,2-ジオール類を、これらの手法を用いれば2つのプロキラルな基質から炭素-炭素結合を形成しながら高立体選択的に合成することができる。 位水酸基の保護基を選択するだけで望みの立体配置を持つ光学活性1,2-ジオールを合成できる、簡便な方法を確立した(第一章・第四節)。従来オレフィン類の不斉酸化法しか良い合成法の知られていない光学活性1,2-ジオール類を、これらの手法を用いれば2つのプロキラルな基質から炭素-炭素結合を形成しながら高立体選択的に合成することができる。 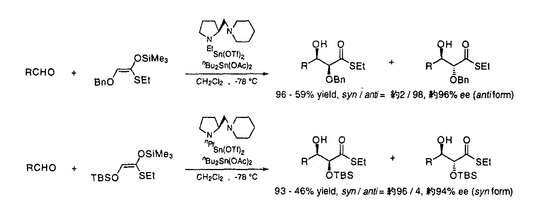 2.抗腫瘍活性化合物タキソールの不斉全合成研究 前章で開発した手法を活用して、天然ポリオキシ化合物であるタキソールの不斉全合成に着手した。タキソールは北米産イチイの樹皮から初めて単離された微量天然物であり、三環性のタキサン骨格のC環にオキセタン部位を有し、8員環であるB環をはさんでA環とC環が向かい合うように折れ曲がった歪の大きなかご形構造をとり、さらにA環にN-ベンゾイルフェニルイソセリン側鎖を有する特異な構造を持っている。 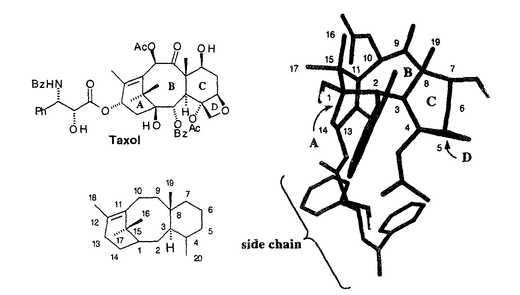 その特徴的な構造は合成標的として多くの有機合成化学者の興味を引き、またその大量供給や類縁体の合成も期待されている。しかし、この化合物の合成は極めて困難で、筆者が合成研究を開始した時点では、発見後20年経過しているにもかかわらずその合成の報告はなかった。筆者はタキソールおよびその類縁体の効率的な全合成法の開発を目指し、まずB環に相当する光学活性なポリオキシ8員環状エノン1を合成し、これにC環部、A環部を順次構築して三環性化合物2とした後、D環に相当するオキセタン部を構築してタキソールへ誘導する合成戦略を考案した。この合成ルートの最大の特徴は、合成困難とされている8員環状骨格を合成の初期の段階で構築する点にある。 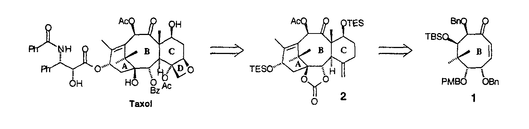 筆者はまずポリオキシ8員環状エノン1の不斉合成を検討し、第一章で開発した不斉アルドール反応あるいはL-セリンを用いるキラルプール法によって光学活性なトリアルコキシアルデヒド3を合成し、これに対するジアステレオ選択的なアルドール反応により光学活性な鎖状ポリオキシエステル4を高収率かつ高立体選択的に得る方法を確立した。このポリオキシエステル4から誘導される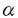 -ブロモメチルケトアルデヒド5にヨウ化サマリウム(II)を作用させると分子内アルドール反応が円滑に進行し、光学活性なポリオキシ8員環状エノン1を収率良く合成することができた(第二章・第二節)。 -ブロモメチルケトアルデヒド5にヨウ化サマリウム(II)を作用させると分子内アルドール反応が円滑に進行し、光学活性なポリオキシ8員環状エノン1を収率良く合成することができた(第二章・第二節)。 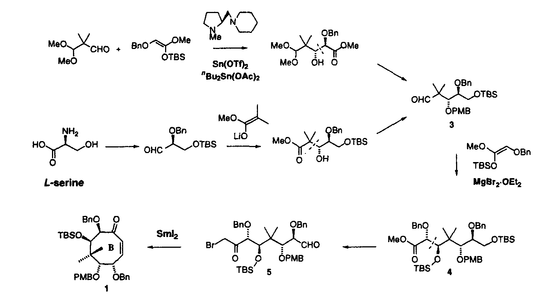 次に、タキソールのC環を構築するためのフラグメントを、B環部にマイケル反応で導入することを考えた。どのような官能基をもつフラグメントを導入すればよいかの知見を得るため、まずタキサン骨格のC環部の官能基変換を天然物由来の化合物を用いて検討した。すなわち、入手可能な天然タキサン化合物である10-デアセチルバッカチンIIIを8工程で新規タキソイド2に誘導し、これに過安息香酸t-ブチルおよび臭化銅(I)を作用させたところ、対応するアリル型の臭化物が高収率で得られることを見い出した。このオレフィン部位をジヒドロキシル化するとジヒドロキシブロミドが得られ、これにDBUを作用させると高収率でオキセタンに誘導できることが明らかになった。次いで種々の位置選択的な保護基の導入法を見出し、7-TESバッカチンIII(6)を良好な収率で合成することができた。6はエステル化によりタキソールへ導くことが可能なので、第二節で述べた合成計画における重要な中間体である8員環状化合物1から上記の新規タキソイド2を合成することができればタキソールの不斉全合成が達成できる(第二章・第三節)。 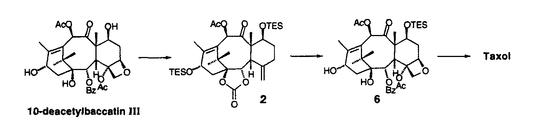 以上の結果から、C環に相当するフラグメントとしては、4-ブロモ-4-ペンテン-1-オールから調製する金属化合物を8員環エノン1ヘマイケル付加させれば良いことがわかった。付加反応は高立体選択的に進行し、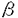 体7を高収率で得ることができた。次いで第一級アルコール部分を酸化しケトアルデヒドとした後、NaOMeを塩基として用いる分子内アルドール反応によって、8-デメチルタキサン系化合物のBC環部位に相当する二環性化合物8を高収率で得ることができた。続いてケトン部位を立体選択的に還元し、生じる1,3-ジオールを保護してアセタールとした後に、A環の構築を試みた。まず、上記のアセタールのPMB基の除去および酸化を行い、8員環状ケトン9を高収率で合成した。アリルリチウムを用いるとアリル化反応が高立体選択的に進行することを見出し、 体7を高収率で得ることができた。次いで第一級アルコール部分を酸化しケトアルデヒドとした後、NaOMeを塩基として用いる分子内アルドール反応によって、8-デメチルタキサン系化合物のBC環部位に相当する二環性化合物8を高収率で得ることができた。続いてケトン部位を立体選択的に還元し、生じる1,3-ジオールを保護してアセタールとした後に、A環の構築を試みた。まず、上記のアセタールのPMB基の除去および酸化を行い、8員環状ケトン9を高収率で合成した。アリルリチウムを用いるとアリル化反応が高立体選択的に進行することを見出し、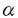 -アリル化物を単一の生成物として得ることができた。次いでTBS基を除去した後、生じる第二級アルコールの酸化ならびにオレフィン部のWacker型酸化を行い、メチルケトン部を有するジケトン10を合成することができた。さらにメチルケトン部を一炭素増炭してエチルケトンに変換することを試みたが、目的物が収率良く得られなかったので、合成計画を次節のように変更した(第二章・第四節)。 -アリル化物を単一の生成物として得ることができた。次いでTBS基を除去した後、生じる第二級アルコールの酸化ならびにオレフィン部のWacker型酸化を行い、メチルケトン部を有するジケトン10を合成することができた。さらにメチルケトン部を一炭素増炭してエチルケトンに変換することを試みたが、目的物が収率良く得られなかったので、合成計画を次節のように変更した(第二章・第四節)。 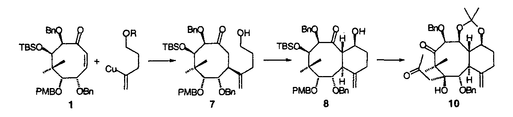 まず、A環フラグメントとしてアリル基ではなくホモアリル基を用いることとし、8員環状ケトン9にホモアリルリチウムを作用し、立体選択的に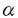 -ホモアリル化体を合成した。次いで新しく見い出した方法により第三級アルコール部分を選択的にシリルエーテルとした後に、Wacker型酸化を経てA環の閉環前駆体となるジケトン11を高収率で得ることができた。ここで低原子価チタン化合物を用いてジケトン11の分子内ピナコール型カップリングを試みたところ、求めるABC骨格を有する三環性化合物12を良好な収率で得ることができた。さらにこの化合物の立体配座を解析し、その配座に有効な反応を選択することにより、この化合物を8-デメチルタキサン系化合物13に導くことができた(第二章・第五節)。 -ホモアリル化体を合成した。次いで新しく見い出した方法により第三級アルコール部分を選択的にシリルエーテルとした後に、Wacker型酸化を経てA環の閉環前駆体となるジケトン11を高収率で得ることができた。ここで低原子価チタン化合物を用いてジケトン11の分子内ピナコール型カップリングを試みたところ、求めるABC骨格を有する三環性化合物12を良好な収率で得ることができた。さらにこの化合物の立体配座を解析し、その配座に有効な反応を選択することにより、この化合物を8-デメチルタキサン系化合物13に導くことができた(第二章・第五節)。 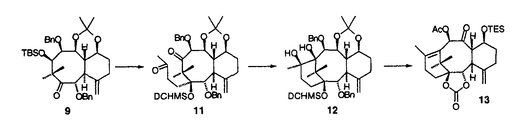 上記の検討で19メチル基のないデメチルタキサン骨格13の構築法を確立することができたので、次にタキソールそのものの合成に取り組んだ。予めタキソール19メチル基を導入した8員環状エノン14をポリオキシ鎖状化合物から効率的に合成し、前述した方法によりタキソールのBC環部に相当する二環性化合物15を高収率で合成した。さらに前節の方法によってA環部の構築ならびに選択的な官能基変換によってタキソール骨格への誘導を行い、タキサン系化合物16を合成する効率的合成ルートを確立した。最後に第三節で述べた手法によりこれにD環部を導入して、7-TESバッカチンIII(6)を合成することができた。一方、著者はA環の側鎖部分であるN-ベンゾイルフェニルイソセリンの不斉合成法とこれと6との脱水縮合法を開発し、タキソールの不斉全合成を完了することができた(第二章・第六節)。 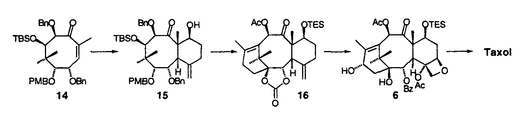 |
| 審査要旨 | | 本論文は、特異な構造をもつ抗癌物質であるタキソールの不斉全合成を達成した結果について述べたものであり,以下の二章から成っている。第一章では,不斉アルドール反応を用いる光学活性1,2-ジオール類の高立体選択的な合成法の開発,第二章では,本不斉アルドールを利用するタキソールの不斉全合成に関して述べている。 第一章:二価スズトリフラート-光学活性ジアミン錯体を用いる不斉アルドール反応 二価スズトリフラート-光学活性ジアミン錯体-四価スズ化合物を不斉触媒に用いることにより,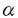 -ベンジルオキシチオ酢酸エステル由来のシリルエノールエーテルとアルデヒドから,ほぼ完全なジアステレオおよびエナンチオ選択性で,アンチ立体配置を有する光学活性な -ベンジルオキシチオ酢酸エステル由来のシリルエノールエーテルとアルデヒドから,ほぼ完全なジアステレオおよびエナンチオ選択性で,アンチ立体配置を有する光学活性な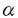 , ,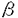 -ジヒドロキシエステル等価体が得られることを見い出した(式1)。一方上記の反応の遷移状態の考察に基づき, -ジヒドロキシエステル等価体が得られることを見い出した(式1)。一方上記の反応の遷移状態の考察に基づき,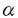 位にかさ高いt-ブチルジメチルシロキシ基をもつチオ酢酸のエノールエーテルを用いて,逆のジアステレオマーであるシン立体配置を有する光学活性 位にかさ高いt-ブチルジメチルシロキシ基をもつチオ酢酸のエノールエーテルを用いて,逆のジアステレオマーであるシン立体配置を有する光学活性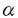 , ,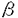 -ジヒドロキシエステルが合成できることを明らかにした(式2)。以上, -ジヒドロキシエステルが合成できることを明らかにした(式2)。以上,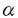 -ヒドロキシチオ酢酸エステルの -ヒドロキシチオ酢酸エステルの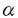 位水酸基の保護基を選択するだけで望みの立体配置を持つ光学活性1,2-ジオールの,簡便な合成法を確立した。 位水酸基の保護基を選択するだけで望みの立体配置を持つ光学活性1,2-ジオールの,簡便な合成法を確立した。 第二章:抗腫瘍活性化合物タキソールの不斉全合成研究 次に著者は前章で開発した手法を活用して,天然ポリオキシ化合物であるタキソールの不斉全合成を行なった。タキソールは,次世代の有望な抗癌剤として期待されるばかりでなく,その特異な構造は合成標的として多くの有機合成化学者の興味を集めている。著者はタキソールおよびその類縁体の効率的な全合成法の開発を目指し,まずB環に相当する光学活性なポリオキシ8員環状エノン1を合成し,これにC環部,A環部を順次構築して三環性化合物2とした後,D環に相当するオキセタン部を構築してタキソールへ誘導する合成戦略を考案した(式3)。 著者はまずポリオキシ8員環状エノン1の不斉合成を検討し,第一章で開発した不斉アルドール反応あるいはL-セリンを用いるキラルプール法によって光学活性なトリアルコキシアルデヒド3を合成し,これに対するジアステレオ選択的なアルドール反応により光学活性な鎖状ポリオキシエステル4を高収率かつ高立体選択的に得る方法を確立した。このポリオキシエステル4から誘導される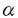 -ブロモメチルケトアルデヒド5にヨウ化サマリウム(II)を作用させ分子内アルドール反応を行い,光学活性なポリオキシ8員環状エノン1を収率良く合成することができた(式4)。 -ブロモメチルケトアルデヒド5にヨウ化サマリウム(II)を作用させ分子内アルドール反応を行い,光学活性なポリオキシ8員環状エノン1を収率良く合成することができた(式4)。 C環部の構築は,4-ブロモ-4-ペンテン-1-オールから調製した銅試剤を8員環エノン1へ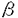 -選択的にマイケル付加させ,次いで第一級アルコール部分を酸化しケトアルデヒドとした後,NaOMeを塩基として用いる分子内アルドール反応によって,8-デメチルタキサン系化合物のBC環部位に相当する二環性化合物6を高収率で得ることができた。続いて,A環フラグメントとしてホモアリル基を導入し,新しく開発した第三級アルコールの選択的なシリル化法や,Wacker型酸化を利用してジケトン7を高収率で得ることができた。ここで低原子価チタン化合物を用いてジケトン7の分子内ピナコール型カップリングを試みたところ,求めるABC骨格を有する三環性化合物8を良好な収率で得ることができ,さらにこの化合物を8-デメチルタキサン系化合物9に導くことができた(式5)。 -選択的にマイケル付加させ,次いで第一級アルコール部分を酸化しケトアルデヒドとした後,NaOMeを塩基として用いる分子内アルドール反応によって,8-デメチルタキサン系化合物のBC環部位に相当する二環性化合物6を高収率で得ることができた。続いて,A環フラグメントとしてホモアリル基を導入し,新しく開発した第三級アルコールの選択的なシリル化法や,Wacker型酸化を利用してジケトン7を高収率で得ることができた。ここで低原子価チタン化合物を用いてジケトン7の分子内ピナコール型カップリングを試みたところ,求めるABC骨格を有する三環性化合物8を良好な収率で得ることができ,さらにこの化合物を8-デメチルタキサン系化合物9に導くことができた(式5)。 上記の検討で19メチル基のないデメチルタキサン骨格9の構築ルートを確立することができたので,次にタキソールそのものの合成に取り組んだ。予めタキソール19メチル基を導入した光学活性8員環状エノン10を合成し,前述した方法によりタキソールのBC環部に相当する二環性化合物11を高収率で合成した。さらにA環部の構築ならびに選択的な官能基変換によってタキソール骨格への誘導を行い,タキサン系化合物12に至る効率的な合成ルートを確立した。最後に新しいオキセタン環形成反応を開発してD環部を導入し,7-TESバッカチンIIIを合成することができた。一方,著者はA環の側鎖部分であるN-ベンゾイルフェニルイソセリンの不斉合成法と,これと7-TESBac catinIIIとの脱水縮合法を開発し,タキソールの不斉全合成を完了することができた(式6)。 以上,本著者は二価スズトリフラート-光学活性ジアミン-四価スズ化合物の組合せからなる複合系不斉触媒を用いる不斉アルドール反応を活用して,種々の光学活性1,2-ジオール類を高立体選択的に合成する手法を開発した。次いでタキソールの全合成に着手し,著者の開発した不斉アルドール反応を利用し従来にない合成戦略に基づきタキソールを合成することに成功した。この業績は有機合成化学の分野に貢献すること大である。なお,本研究は数名による共同研究であるが論文提出者が主体となって開発研究を行なったものであり,論文提出者の寄与は十分であるとする。従って博士(理学)を授与できると認める。 |