G-CSF(顆粒球コロニー刺激因子)は顆粒球系前駆細胞の増殖、分化および成熟好中球の機能を調節する因子である。近年、コロニー刺激因子が破骨細胞の形成に関与することが明らかにされつつあるが、G-CSFの骨への作用については知見が極めて少なく、その詳細は明らかにされていない。申請者の研究の目的は、ラットおよびマウスへ遺伝子組換えヒトG-CSF(rhG-CSF)を投与し、G-CSFの骨への作用を明らかにすることである。論文は以下の6章からなる。 第1章では、ラットにrhG-CSFを28日間投与し、骨変化の病理学的特徴を検討した。その結果、高用量(100および1,000 g/kg)群では、造血系の変化に加え、破骨細胞性骨吸収の亢進と膜内骨化による骨形成を特徴とする骨変化が用量依存性に認められた。骨変化は、骨幹端の海綿骨など生理的に活発な骨吸収が行われている部位に認められた。これらの結果より、高用量のrhG-CSFは造血系とともに骨に作用し、形態変化を誘導することが明らかにされた。 g/kg)群では、造血系の変化に加え、破骨細胞性骨吸収の亢進と膜内骨化による骨形成を特徴とする骨変化が用量依存性に認められた。骨変化は、骨幹端の海綿骨など生理的に活発な骨吸収が行われている部位に認められた。これらの結果より、高用量のrhG-CSFは造血系とともに骨に作用し、形態変化を誘導することが明らかにされた。 第2章では、骨変化と骨成長との関連を、成長期(6週齢)と成長の緩やかな時期(14週齢)のラットにrhG-CSFを28日間投与することにより検討した。その結果、6週齢ラットでは100 g/kg以上の群に、14週齢ラットでは1,000 g/kg以上の群に、14週齢ラットでは1,000 g/kg群にのみに骨変化が認められた。骨変化の程度は6週齢の方が高かった。これらの結果より、成長期のラットは成長の緩やかな時期のラットに比べて骨変化が形成されやすく、rhG-CSF投与に伴う骨変化には骨の生理的状態が深く関与することが明らにされた。 g/kg群にのみに骨変化が認められた。骨変化の程度は6週齢の方が高かった。これらの結果より、成長期のラットは成長の緩やかな時期のラットに比べて骨変化が形成されやすく、rhG-CSF投与に伴う骨変化には骨の生理的状態が深く関与することが明らにされた。 第3章では、骨変化と骨髄造血状態との関連を検討した。ラットに1,000 g/kgのrhG-CSFを28日間投与したところ、骨変化は骨髄の造血状態と密接に関連していることが明らかになった。また、造血が活発な骨髄内では高用量のrhG-CSF投与により破骨細胞前駆細胞の供給が亢進している可能性が示唆された。 g/kgのrhG-CSFを28日間投与したところ、骨変化は骨髄の造血状態と密接に関連していることが明らかになった。また、造血が活発な骨髄内では高用量のrhG-CSF投与により破骨細胞前駆細胞の供給が亢進している可能性が示唆された。 第4章では、骨変化形成過程の経時観察を行い、さらに破骨細胞性骨吸収を抑制するビスフォスフォネート(BP)を併用投与し、骨変化の病理発生を検討した。ラットに1,000 g/kgのrhG-CSFを1〜28日間投与し、経時的に観察した結果、骨吸収の亢進が投与3日後から、骨形成が投与7日後から認められた。いずれの投与期間でも骨吸収が骨形成の発現頻度を常に上回っていた。また、ラットにBPを前処置した後、1,000 g/kgのrhG-CSFを1〜28日間投与し、経時的に観察した結果、骨吸収の亢進が投与3日後から、骨形成が投与7日後から認められた。いずれの投与期間でも骨吸収が骨形成の発現頻度を常に上回っていた。また、ラットにBPを前処置した後、1,000 g/kgのrhG-CSFを14日間投与した結果、破骨細胞性骨吸収の抑制とともに膜内骨化による骨形成も抑制された。これらの結果より、まず破骨細胞性骨吸収の亢進が先行し、その後、カップリング機構に基づく膜内骨化による骨形成が起こることが明らかにされた。 g/kgのrhG-CSFを14日間投与した結果、破骨細胞性骨吸収の抑制とともに膜内骨化による骨形成も抑制された。これらの結果より、まず破骨細胞性骨吸収の亢進が先行し、その後、カップリング機構に基づく膜内骨化による骨形成が起こることが明らかにされた。 第5章では、ラットに1,000 g/kgのrhG-CSFを4〜28日間投与し、骨髄微小環境の変化を検討した。その結果、rhG-CSF投与により骨髄間質細胞および細胞外マトリックスの構成・分布が変化し、破骨細胞の形成および活性化を亢進する骨髄微小環境が構築されることが示された。また、骨髄間質細胞では、ED-1(単球/マクロファージ/樹状細胞系マーカー抗原)陽性、酸ホスファターゼ陽性、ED-2(マクロファージマーカー抗原)陰性の細網細胞様細胞、ならびに、アルカリホスファターゼ陽性および/あるいは g/kgのrhG-CSFを4〜28日間投与し、骨髄微小環境の変化を検討した。その結果、rhG-CSF投与により骨髄間質細胞および細胞外マトリックスの構成・分布が変化し、破骨細胞の形成および活性化を亢進する骨髄微小環境が構築されることが示された。また、骨髄間質細胞では、ED-1(単球/マクロファージ/樹状細胞系マーカー抗原)陽性、酸ホスファターゼ陽性、ED-2(マクロファージマーカー抗原)陰性の細網細胞様細胞、ならびに、アルカリホスファターゼ陽性および/あるいは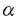 -平滑筋アクチン陽性の線維芽細胞様細胞が、また、細胞外マトリックスではフィブロネクチン、I型コラーゲンおよびヘパラン硫酸プロテオグリカンが骨吸収の過程で重要な役割を果たしていることが明らかにされた。 -平滑筋アクチン陽性の線維芽細胞様細胞が、また、細胞外マトリックスではフィブロネクチン、I型コラーゲンおよびヘパラン硫酸プロテオグリカンが骨吸収の過程で重要な役割を果たしていることが明らかにされた。 第6章では、M-CSFの産生欠乏により大理石骨病を起こすop/opマウスに、rhG-CSFを28日間反復皮下投与し、骨病態の変化を検討した。その結果、rhG-CSF投与群に用量に依存した一次海綿骨長の短縮など病態の改善が認められ、G-CSFがM-CSFの関与しない経路での骨への作用を有することが示唆された。 以上、本研究により、高用量のG-CSF投与は骨に破骨細胞性骨吸収の亢進と膜内骨化による骨形成を特徴とする形態変化を起こすことが明らかにされた。また、骨吸収の亢進が先行し、その後、カップリング機構に基づく骨形成が起こるという病理発生機序が示された。さらに、高用量のG-CSFが破骨細胞系細胞の供給を亢進させ、同時に、骨髄間質細胞および細胞外マトリックスの構成・分布を変化させて、破骨細胞の形成および活性化を亢進する骨髄微小環境を構築することが明らかにされた。このように、本研究の成果は、G-CSFによる、より普遍的な骨および骨髄の形態および機能の調節機構を明らかにしていく上で極めて重要であると考えられ、造血器、骨研究の推進に寄与するところが大きいと考えられる。したがって、審査委員一同は本論文が博士(獣医学)の学位論文として価値あるものと認めた。 |