| (始めに) TNF- は生体防御・免疫機構に広く関わるサイトカインであり免疫機能亢進作用や抗腫瘍作用等有益な作用を示す一方で、発癌プロモーション作用や悪液質の誘導等有害な作用をも併せ持つ。そこで、TNF- は生体防御・免疫機構に広く関わるサイトカインであり免疫機能亢進作用や抗腫瘍作用等有益な作用を示す一方で、発癌プロモーション作用や悪液質の誘導等有害な作用をも併せ持つ。そこで、TNF- の産生をある局面では促進し、又他の局面では抑制し得るような薬物開発がTNF- の産生をある局面では促進し、又他の局面では抑制し得るような薬物開発がTNF- を標的とした生物応答調節剤創製の観点から、又TNF- を標的とした生物応答調節剤創製の観点から、又TNF- の産生制御機構解明の観点から重要と考えた。 の産生制御機構解明の観点から重要と考えた。 リード化合物として"サリドマイド"に着目した。サリドマイドは催奇形性の副作用のために市場撤退した催眠剤であるが、決して過去の歴史の中に葬られた医薬ではなく、現在その有用性が再認識され再び注目されている薬物である。そしてその作用はTNF- の産生調節にあるとされている。サリドマイドの催奇形性については未だ明快な科学的解答が無いが、その高い種特異性から代謝物が催奇形性発現の本体である疑いが濃い。サリドマイドの有効な薬効がTNF- の産生調節にあるとされている。サリドマイドの催奇形性については未だ明快な科学的解答が無いが、その高い種特異性から代謝物が催奇形性発現の本体である疑いが濃い。サリドマイドの有効な薬効がTNF- 産生調節活性にあるのならば、この活性を指標にしての"ニューサリドマイド"の創製が可能であると考えた。 産生調節活性にあるのならば、この活性を指標にしての"ニューサリドマイド"の創製が可能であると考えた。 (サリドマイドの二方向性TNF- 産生調節作用) 産生調節作用) サリドマイドはTNF- 産生を抑制するとの報告が多いが、必ずしも定量性、再現性のある実験系で認められたものではない。そこで評価系の構築から着手した。迅速かつ安定した結果の得られる一次評価系が必要である事から、培養白血病細胞株のHL-60を選択した。刺激剤には代表的発癌プロモータ-を検討した。HL-60は発癌プロモータ-刺激に鋭敏に反応しTNF- 産生を抑制するとの報告が多いが、必ずしも定量性、再現性のある実験系で認められたものではない。そこで評価系の構築から着手した。迅速かつ安定した結果の得られる一次評価系が必要である事から、培養白血病細胞株のHL-60を選択した。刺激剤には代表的発癌プロモータ-を検討した。HL-60は発癌プロモータ-刺激に鋭敏に反応しTNF- 産生を示したので、応答の良いTPA及びオカダ酸(OA)を用いた評価系を構築した。この評価系を用いてサリドマイドを検定すると、サリドマイドが刺激剤及び細胞種特異的な二方向性のTNF- 産生を示したので、応答の良いTPA及びオカダ酸(OA)を用いた評価系を構築した。この評価系を用いてサリドマイドを検定すると、サリドマイドが刺激剤及び細胞種特異的な二方向性のTNF- 産生調節作用を示す事を見出した。TPA/HL-60系ではTNF- 産生調節作用を示す事を見出した。TPA/HL-60系ではTNF- 産生促進剤として作用し、OA/HL-60系では産生抑制剤として作用している。しかし他の白血病細胞株であるTHP-1の場合には何れの刺激剤を用いても産生抑制作用を示した。 産生促進剤として作用し、OA/HL-60系では産生抑制剤として作用している。しかし他の白血病細胞株であるTHP-1の場合には何れの刺激剤を用いても産生抑制作用を示した。 (サリドマイドの構造展開) これらの知見を踏まえて更に強力なTNF- 産生調節剤の創製を目指した。構造展開戦略は、サリドマイドの催奇形性にはグルタルイミド環部分の構造とその代謝物に依存する事が推定されていたので、N-フェニルフタルイミドを基本とする構造修飾を行った。その結果、ベンゼン環の二つのオルト位への疎水性の嵩高い置換基導入がTNF- 産生調節剤の創製を目指した。構造展開戦略は、サリドマイドの催奇形性にはグルタルイミド環部分の構造とその代謝物に依存する事が推定されていたので、N-フェニルフタルイミドを基本とする構造修飾を行った。その結果、ベンゼン環の二つのオルト位への疎水性の嵩高い置換基導入がTNF- 産生調節作用には重要である事が判明した。特に2,6-ジイソプロピル体17はサリドマイドを遥かに凌ぐTNF- 産生調節作用には重要である事が判明した。特に2,6-ジイソプロピル体17はサリドマイドを遥かに凌ぐTNF- 産生調節剤であった。興味深い化合物は17をテトラフルオロ化した23である。この化合物はナノモルオーダーの薬用量でTNF- 産生調節剤であった。興味深い化合物は17をテトラフルオロ化した23である。この化合物はナノモルオーダーの薬用量でTNF- の産生調節作用を示した。この様にして活性の強度という点からは概ね満足できる化合物を創製する事に成功した。 の産生調節作用を示した。この様にして活性の強度という点からは概ね満足できる化合物を創製する事に成功した。 (二方向性TNF- 産生調節作用の構造展開による分離) 産生調節作用の構造展開による分離) 今後の医薬化学及び作用機構研究の観点から重要な次なる課題は二方向性調節作用の分離にある。フタルイミド誘導体のTNF- 産生調節作用の構造活性相関は類似しており、平面的な分子の形状変換による作用の分離には限界を感じ、化合物の電子的性質の変換による作用の分離を期待した。その結果、産生促進に関しては電子吸引性のニトロ基の導入により活性が向上し、電子供与性基の導入は活性を落とした。逆に産生抑制に関しては電子吸引性基の導入は活性を下げ、一方特に5位へ電子供与性の水酸基の導入が抑制活性を向上させる事が判明した。このように電子的性質の変換により二方向性調節作用をある程度分離した化合物を得る事に成功した。これらの結果は、産生促進と産生抑制の各系で化合物の形状や電子的な性質が厳密に認識されている、即ち、別々の薬物受容体が存在する事を示唆していると考える。一般に薬物受容体は光学活性な生体内高分子である。そこで光学活性な化合物をデザインする事により作用の特異性を上昇させ得ると考えた。 産生調節作用の構造活性相関は類似しており、平面的な分子の形状変換による作用の分離には限界を感じ、化合物の電子的性質の変換による作用の分離を期待した。その結果、産生促進に関しては電子吸引性のニトロ基の導入により活性が向上し、電子供与性基の導入は活性を落とした。逆に産生抑制に関しては電子吸引性基の導入は活性を下げ、一方特に5位へ電子供与性の水酸基の導入が抑制活性を向上させる事が判明した。このように電子的性質の変換により二方向性調節作用をある程度分離した化合物を得る事に成功した。これらの結果は、産生促進と産生抑制の各系で化合物の形状や電子的な性質が厳密に認識されている、即ち、別々の薬物受容体が存在する事を示唆していると考える。一般に薬物受容体は光学活性な生体内高分子である。そこで光学活性な化合物をデザインする事により作用の特異性を上昇させ得ると考えた。 サリドマイドはラセミ体で用いられ、光学活性と薬理作用の関係が議論されていた。化学的には不斉炭素に結合した水素の産生は高く容易にラセミ化が起こると考えられ、実際通常の生物検定系では光学活性体間の生物作用の差を検出できなかった。そこで光学的に安定な光学活性メチルサリドマイドを合成して調べると、TPA/HL-60系では(S)-体のみが促進活性を示し(R)-体は不活性である事が、一方OA/HL-60系では(R)-体の方が(S)-体よりも強い抑制活性を示すという二方向性調節作用の立体選択性を示す事を見出した。光学活性の導入により作用の完全分離の可能性を示す事ができたので、これまでの構造活性相関の知見を踏まえ更なる構造修飾を行った。作用増強の期待されるテトラフルオロフタルイミド骨格を有する光学活性化合物を評価するとやはり二方向性調節作用の立体選択性が認められた。特に33や35は0.3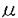 Mという低濃度でTNF- Mという低濃度でTNF- の産生をほぼ完全に抑制し、同薬用量で促進活性を示さない優れたTNF- の産生をほぼ完全に抑制し、同薬用量で促進活性を示さない優れたTNF- 産生抑制剤であった。一方42はTNF- 産生抑制剤であった。一方42はTNF- の産生抑制作用を示さない強力なTNF- の産生抑制作用を示さない強力なTNF- 産生促進剤であった。これらの化合物を見出した事により、TNF- 産生促進剤であった。これらの化合物を見出した事により、TNF- 産生調節機構解析の上でも、又TNF- 産生調節機構解析の上でも、又TNF- を標的とする生物応答調節剤開発を行う上でも優れたプローブ或いはリードを提供できたと考える。二方向性の作用機構としては薬物受容体として産生促進に関与する因子と、それとは別の抑制に関与する因子の存在を考える事により説明できると考えている。現在この仮想的蛋白性因子の候補の探索を行っている。手法としては作用の特異性に優れた33と34をリガンドとするアフィニティゲルを調製し、それに結合する蛋白を探索するという方法を試みている。SDS-PAGEからは、(R)-体と(S)-体由来のゲルの両方に特異的結合が認められるバンド、片方のみに特異的に認められるバンド等が検出されている。これらの蛋白質がTNF- を標的とする生物応答調節剤開発を行う上でも優れたプローブ或いはリードを提供できたと考える。二方向性の作用機構としては薬物受容体として産生促進に関与する因子と、それとは別の抑制に関与する因子の存在を考える事により説明できると考えている。現在この仮想的蛋白性因子の候補の探索を行っている。手法としては作用の特異性に優れた33と34をリガンドとするアフィニティゲルを調製し、それに結合する蛋白を探索するという方法を試みている。SDS-PAGEからは、(R)-体と(S)-体由来のゲルの両方に特異的結合が認められるバンド、片方のみに特異的に認められるバンド等が検出されている。これらの蛋白質がTNF- 産生制御機構の中枢に位置している事を期待して実験を進めている。 産生制御機構の中枢に位置している事を期待して実験を進めている。 (TNF- 産生調節剤の抗アンドロゲン作用) 産生調節剤の抗アンドロゲン作用) TNF- は内因性の発癌プロモーターであると報告されている。一方、重要な内因性発癌プロモーターとしてアンドロゲンやエストロゲンがある。近年、ホルモン依存性の癌患者が増加し、抗ホルモン剤の癌治療への展開が図られている。例えば乳癌治療に抗エストロゲン剤のタモキシフェンが用いられている。更にタモキシフェンにはTNF- は内因性の発癌プロモーターであると報告されている。一方、重要な内因性発癌プロモーターとしてアンドロゲンやエストロゲンがある。近年、ホルモン依存性の癌患者が増加し、抗ホルモン剤の癌治療への展開が図られている。例えば乳癌治療に抗エストロゲン剤のタモキシフェンが用いられている。更にタモキシフェンにはTNF- 産生抑制作用も認められ、タモキシフェンの抗癌剤としての有効性にこの作用も寄与していると推測されている。それならば抗アンドロゲン剤もTNF- 産生抑制作用も認められ、タモキシフェンの抗癌剤としての有効性にこの作用も寄与していると推測されている。それならば抗アンドロゲン剤もTNF- 産生抑制作用を合わせ持てばより有効な前立腺癌治療薬になるのではないかと考えた。そこで抗アンドロゲン剤フルタミドのTNF- 産生抑制作用を合わせ持てばより有効な前立腺癌治療薬になるのではないかと考えた。そこで抗アンドロゲン剤フルタミドのTNF- 産生抑制作用を調べたが活性は認められなかった。ところで、TNF- 産生抑制作用を調べたが活性は認められなかった。ところで、TNF- とアンドロゲンはその生物活性に類似性が見て取れる。又フタルイミド誘導体は非ステロイド性抗アンドロゲン剤と構造上の類似性も認められる。そこでこれらのフタルイミド誘導体中に抗アンドロゲン作用を示す化合物がある事を期待した。活性評価はCATアッセイによるアンドロゲン受容体の活性化阻害効果、及びアンドロゲン依存的に増殖するSC-3細胞の増殖抑制効果を観ることで行った。その結果、テトラフルオロフタルイミド誘導体の中にフルタミド以上の抗アンドロゲン作用を示す化合物がある事が判明した。CATアッセイの結果とSC-3の増殖抑制は良い相関を示しており、これらの化合物はフルタミドと同様核内アンドロゲン受容体に直接作用する拮抗薬であると推測する。 とアンドロゲンはその生物活性に類似性が見て取れる。又フタルイミド誘導体は非ステロイド性抗アンドロゲン剤と構造上の類似性も認められる。そこでこれらのフタルイミド誘導体中に抗アンドロゲン作用を示す化合物がある事を期待した。活性評価はCATアッセイによるアンドロゲン受容体の活性化阻害効果、及びアンドロゲン依存的に増殖するSC-3細胞の増殖抑制効果を観ることで行った。その結果、テトラフルオロフタルイミド誘導体の中にフルタミド以上の抗アンドロゲン作用を示す化合物がある事が判明した。CATアッセイの結果とSC-3の増殖抑制は良い相関を示しており、これらの化合物はフルタミドと同様核内アンドロゲン受容体に直接作用する拮抗薬であると推測する。 一方、抗アンドロゲン作用とTNF- 産生抑制作用の相関は乏しい。例えば、強い抗アンドロゲン作用を示した34,36は0.3 産生抑制作用の相関は乏しい。例えば、強い抗アンドロゲン作用を示した34,36は0.3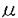 Mの薬用量ではTNF- Mの薬用量ではTNF- 産生抑制作用を示さなかった。更にTNF- 産生抑制作用を示さなかった。更にTNF- 産生抑制作用には明確な立体選択性が認められるが、抗アンドロゲン作用には立体選択性は認められず、各エナンチオマーとも同等の抗アンドロゲン作用を示した。 産生抑制作用には明確な立体選択性が認められるが、抗アンドロゲン作用には立体選択性は認められず、各エナンチオマーとも同等の抗アンドロゲン作用を示した。 強いTNF- 産生抑制作用を示す33,35及び37には抗アンドロゲン作用も認めらた。アンドロゲンもTNF- 産生抑制作用を示す33,35及び37には抗アンドロゲン作用も認めらた。アンドロゲンもTNF- も共に癌の増悪因子である事を考えると、これらの化合物は"抗アンドロゲン作用とTNF- も共に癌の増悪因子である事を考えると、これらの化合物は"抗アンドロゲン作用とTNF- 産生抑制作用の両作用を合わせ持つ新規前立腺癌治療薬"という新しいコンセプトの抗癌剤のプロトタイプとして興味深いと考えている。 産生抑制作用の両作用を合わせ持つ新規前立腺癌治療薬"という新しいコンセプトの抗癌剤のプロトタイプとして興味深いと考えている。 (まとめ) 以上私は新規生物応答調節剤の創製を目的としてサリドマイドに着目し、構造修飾を展開した結果、ナノモルオーダーの薬用量で二方向TNF- 産生調節作用を示すテトラフルオロフタルイミド誘導体を見出した。 産生調節作用を示すテトラフルオロフタルイミド誘導体を見出した。 またこれらの化合物のTNF- 産生調節に関わる二方向性の作用の分離にも成功し、TNF- 産生調節に関わる二方向性の作用の分離にも成功し、TNF- 産生抑制活性のみをもつテトラフルオロフタルイミド誘導体及び選択的なTNF- 産生抑制活性のみをもつテトラフルオロフタルイミド誘導体及び選択的なTNF- 産生促進活性のみをもつテトラフルオロフタルイミド誘導体をそれぞれ創製した。 産生促進活性のみをもつテトラフルオロフタルイミド誘導体をそれぞれ創製した。 更にはTNF- 産生調節剤中に抗アンドロゲン作用を示す化合物をも見出した。これらのフタルイミド系生物応答調節剤をプローブとしたTNF- 産生調節剤中に抗アンドロゲン作用を示す化合物をも見出した。これらのフタルイミド系生物応答調節剤をプローブとしたTNF- の産生制御機構解明という基礎研究及び医薬としての応用研究が期待される。 の産生制御機構解明という基礎研究及び医薬としての応用研究が期待される。 |