傷害を受けた組織を修復するという創傷治癒は、生物の生存にとって非常に重要なプロセスである。その創傷治癒が細胞学的及び分子生物学的なメカニズムによって高度に調節され達成されるということは明らかである。サイトカインTransforming Growth Factor-alpha( )とTransforming Growth Factor-beta1( )とTransforming Growth Factor-beta1(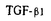 )は、創傷治癒に関与する重要な調節因子であるといわれ広く研究がなされている。また好酸球は、皮膚の創傷治癒の炎症巣において観察されるということが報告されているが、その存在の重要性についての詳しい見解には今だ不明な点が残っている。 )は、創傷治癒に関与する重要な調節因子であるといわれ広く研究がなされている。また好酸球は、皮膚の創傷治癒の炎症巣において観察されるということが報告されているが、その存在の重要性についての詳しい見解には今だ不明な点が残っている。 Todd及びWongらは、好酸球が皮膚や口腔粘膜における創傷治癒の過程で、サイトカイン 及び 及び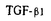 の両者を発現していることを初めて明らかにすることに成功した(Todd et al.,Am J Path138,1307-1313,1991;Wong et al.,Blood78,2702-2707,1991)。注目すべきことに、創傷治癒の際の好酸球において、毛細血管新生や上皮細胞の遊走や増殖という役割を担う の両者を発現していることを初めて明らかにすることに成功した(Todd et al.,Am J Path138,1307-1313,1991;Wong et al.,Blood78,2702-2707,1991)。注目すべきことに、創傷治癒の際の好酸球において、毛細血管新生や上皮細胞の遊走や増殖という役割を担う の発現が、創傷周囲で線維性結合組織の形成に関与している の発現が、創傷周囲で線維性結合組織の形成に関与している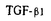 のそれに先行するのである(Wong et al.,Am J Path143,130-142,1993)。好酸球において、この2つのサイトカイン のそれに先行するのである(Wong et al.,Am J Path143,130-142,1993)。好酸球において、この2つのサイトカイン と と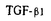 が連続的に発現されるという興味深い事実から、好酸球が創傷治癒の過程において重要な役割を担っていると考られた。 が連続的に発現されるという興味深い事実から、好酸球が創傷治癒の過程において重要な役割を担っていると考られた。 またElovicらは、ヒト好酸球において、サイトカインInterleukin-4(IL-4)が の発現を抑制し、それと同時に、 の発現を抑制し、それと同時に、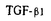 の発現を促進することをin-situハイブリダイゼーションおよび免疫組織染色法を用いて明らかにした(Elovic et al.,J Aller and Clin Immun93,864-869,1994)。そのためIL-4が、好酸球内で創傷治癒の前半期、 の発現を促進することをin-situハイブリダイゼーションおよび免疫組織染色法を用いて明らかにした(Elovic et al.,J Aller and Clin Immun93,864-869,1994)。そのためIL-4が、好酸球内で創傷治癒の前半期、 の発現を促進し、後半期において の発現を促進し、後半期において の発現を抑制し、一方で の発現を抑制し、一方で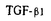 の発現を促進するというプロモーター的な役割を果しているのではないかと推察された。Kucukcelebiらによる近年の、IL-4の塗布が創傷の治癒を早めるという興味深い報告は、創傷治癒におけるIL-4の重要性を支持するものである(Kucukcelebi et al.,J of Wound Healing3,49-58,1995)。また、IL-4は創傷治癒の際に浸潤してくる種々の細胞(T細胞、肥満細胞そして一部のB細胞など)に於いて分泌されるという事実を考慮すると、IL-4が、好酸球内における の発現を促進するというプロモーター的な役割を果しているのではないかと推察された。Kucukcelebiらによる近年の、IL-4の塗布が創傷の治癒を早めるという興味深い報告は、創傷治癒におけるIL-4の重要性を支持するものである(Kucukcelebi et al.,J of Wound Healing3,49-58,1995)。また、IL-4は創傷治癒の際に浸潤してくる種々の細胞(T細胞、肥満細胞そして一部のB細胞など)に於いて分泌されるという事実を考慮すると、IL-4が、好酸球内における 及び 及び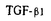 発現の分子生物学的スイッチ(Molecular swich)という重要な役割を果しているという可能性が考えられた。 発現の分子生物学的スイッチ(Molecular swich)という重要な役割を果しているという可能性が考えられた。 そこで、好酸球の と と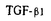 を発現するという創傷治癒における生物学的重要性、またIL-4の創傷治癒における生物学的重要性を解析するため、 を発現するという創傷治癒における生物学的重要性、またIL-4の創傷治癒における生物学的重要性を解析するため、 と と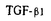 の遺伝子発現のIL-4による分子生物学的調節機構を検討することとし、次の様な仮説をたてた。 の遺伝子発現のIL-4による分子生物学的調節機構を検討することとし、次の様な仮説をたてた。 遺伝子のプロモーター部分に存在する、IL-4に特異的な既知(TTC-(X)n-GAA)もしくは未知のDNA結合ドメインに応答する特異的転写因子、IL-4についてはこれまでIL-4 NAF/STF-IL-4(STAT6)及び4PS(IRS-2)の2つが確認されているのであるが、それらの転写因子をIL-4が誘導又は抑制し、その結果 遺伝子のプロモーター部分に存在する、IL-4に特異的な既知(TTC-(X)n-GAA)もしくは未知のDNA結合ドメインに応答する特異的転写因子、IL-4についてはこれまでIL-4 NAF/STF-IL-4(STAT6)及び4PS(IRS-2)の2つが確認されているのであるが、それらの転写因子をIL-4が誘導又は抑制し、その結果 遺伝子発現が抑制される。 遺伝子発現が抑制される。 この仮説を検討するため、ヒト 遺伝子のプロモーター領域をクローニングし、そしてシークエンス反応を行ないこのプロモーター部分の塩基配列を確認した。そのクローニングされたヒト 遺伝子のプロモーター領域をクローニングし、そしてシークエンス反応を行ないこのプロモーター部分の塩基配列を確認した。そのクローニングされたヒト プロモーターを、Luciferase Reporter Vector;pGL3-Basicに組み込みHuman プロモーターを、Luciferase Reporter Vector;pGL3-Basicに組み込みHuman Luciferase Vector;pGL3-hu Luciferase Vector;pGL3-hu Pを構築した。プロモーター部分の既知のIL-4特異的DNA結合ドメイン(TTC-(X)n-GAA)についての分析を行い、重要な所見として、少なくとも-1262,-1139,-987の3つの部位に既知のIL-4特異的DNA結合ドメインが位置しており、興味深いことにこれらの3つの部位は転写開始部位の約1-kb上流域に位置し、283-bp内に限局する可能性が示された。また、転写因子NF Pを構築した。プロモーター部分の既知のIL-4特異的DNA結合ドメイン(TTC-(X)n-GAA)についての分析を行い、重要な所見として、少なくとも-1262,-1139,-987の3つの部位に既知のIL-4特異的DNA結合ドメインが位置しており、興味深いことにこれらの3つの部位は転写開始部位の約1-kb上流域に位置し、283-bp内に限局する可能性が示された。また、転写因子NF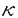 B及びC/EBPもIL-4のシグナル伝達系に関与しているという報告があり、少なくとも3つのNF B及びC/EBPもIL-4のシグナル伝達系に関与しているという報告があり、少なくとも3つのNF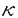 Bの結合ドメイン、1つのC/EBP結合ドメインがヒト Bの結合ドメイン、1つのC/EBP結合ドメインがヒト プロモーター部位に位置することが示唆された。 プロモーター部位に位置することが示唆された。 ヒト好酸球を研究する際の重大な問題点は、in vitroにおいて十分な細胞を獲得することが難しいことである。そのため、分子生物学的、細胞学的にヒト好酸球の研究は非常に困難であり、本研究のための適した細胞群を検討することは重要なことである。EoL-1細胞は、ヒト好酸球としては現在唯一樹立されている細胞株であり、京都大学の真弓博士より供与していただいた。まず、このEoL-1細胞の本研究に対する分子生物学的特徴を検討した。ヒト正常好酸球と同様にEoL-1細胞は 及び 及び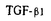 を発現するが、IL-4は発現しない。また、EoL-1細胞の約20%が、ヒト成熟好酸球特有のRhodamine fluorescence(Wong et al.,J Exp Med172,673-81,1990;Wong et al.,Blood 78,2702-2707,1991)の特徴を示した。 を発現するが、IL-4は発現しない。また、EoL-1細胞の約20%が、ヒト成熟好酸球特有のRhodamine fluorescence(Wong et al.,J Exp Med172,673-81,1990;Wong et al.,Blood 78,2702-2707,1991)の特徴を示した。 またIL-4は細胞膜上の特異的レセプターに結合して初めてその生理活性を発揮するので、IL-4レセプターの発現の有無を確認することは意義がある。RT-PCR法及びフローサイトメトリー法により、IL-4レセプターの発現を正常ヒト好酸球とEoL-1細胞において確認し、両者ともに外来からのIL-4に対して応答する可能性を示した。さらに、既知のIL-4特異的転写因子STAT6、4PS(IRS-2)が正常ヒト好酸球とEoL-1細胞において存在することをWestern Blot法を用いて確認した。現在までにヒト好酸球とヒト好酸球様細胞EoL-1細胞において、IL-4レセプター及びIL-4特異的転写因子を検討した報告例はなく、本研究において初めて正常ヒト好酸球とEoL-1細胞内でIL-4シグナル伝達系が存在する可能性を示唆することとなった。そして、この細胞株においても、ヒトの正常好酸球でみられるのと同様に外来性のIL-4に応答して の発現抑制と の発現抑制と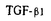 の発現促進が起こることをRT-PCR法により確認したため、IL-4によるヒト の発現促進が起こることをRT-PCR法により確認したため、IL-4によるヒト 遺伝子のプロモーターを解析するために、このEoL-1は最適な細胞と考えられた。また過去に、この細胞株を用いた遺伝子導入法についての報告はなく、本研究において、エレクトロポレーション(電気的パルスによる遺伝子導入法)による遺伝子導入法の確立に成功した(Ohyama et al.,J Immunol Meth,in press,1998)。 遺伝子のプロモーターを解析するために、このEoL-1は最適な細胞と考えられた。また過去に、この細胞株を用いた遺伝子導入法についての報告はなく、本研究において、エレクトロポレーション(電気的パルスによる遺伝子導入法)による遺伝子導入法の確立に成功した(Ohyama et al.,J Immunol Meth,in press,1998)。 ヒト好酸球における 遺伝子発現を検討するためにルシフェラーゼ遺伝子をレポーター遺伝子として用い、今回構築されたヒト 遺伝子発現を検討するためにルシフェラーゼ遺伝子をレポーター遺伝子として用い、今回構築されたヒト 遺伝子のプロモーター(pGL3-hu 遺伝子のプロモーター(pGL3-hu P)の転写活性をEoL-1細胞において確認したのであるが、アクティベーター/エンハンサー配列がプロモーターの-1600から-1400の間に存在している可能性があるという興味深い所見を得た。アクティベーター/エンハンサーの正確な位置及びそれに結合する転写因子の同定など、さらなる探究が期待される。 P)の転写活性をEoL-1細胞において確認したのであるが、アクティベーター/エンハンサー配列がプロモーターの-1600から-1400の間に存在している可能性があるという興味深い所見を得た。アクティベーター/エンハンサーの正確な位置及びそれに結合する転写因子の同定など、さらなる探究が期待される。 このように、好酸球、好酸球由来の 、 、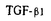 およびIL-4が創傷治癒に重要な関わりを持っていると推察されるが、これまでに体系的にそれらの関連性について研究がなされた報告例はなく、本研究により初めて生物学的に重要な2つのサイトカイン およびIL-4が創傷治癒に重要な関わりを持っていると推察されるが、これまでに体系的にそれらの関連性について研究がなされた報告例はなく、本研究により初めて生物学的に重要な2つのサイトカイン 及びIL-4を関連づけることなった。ここに報告した実験結果を通して、ヒト好酸球における 及びIL-4を関連づけることなった。ここに報告した実験結果を通して、ヒト好酸球における 遺伝子発現を解析するためのin vitroにおける実験モデルが確立されたと考えられる。 遺伝子発現を解析するためのin vitroにおける実験モデルが確立されたと考えられる。 |