| 【序】 個体発生や生体の恒常性の維持において、細胞死は重要な生理現象のひとつである。実際、多細胞動物の発生過程では、細胞が分化、増殖するだけでなく、特定の時期に特定の細胞が死ぬ"プログラム細胞死"という現象が観察される。遺伝的にプログラムされた細胞死は、染色体や細胞質の凝縮、細分化を伴う。そして死に至った細胞は最終的には食細胞に捉えられ、周りに影響を及ぼさずに消滅する。このような細胞死のことを形態学的に、アポトーシスという。それに対して、外部からの傷害や刺激により引き起こされる言わば偶発的な細胞死(事故死:accidental cell death)では、細胞膜の裂傷、細胞内物質の流出が認められる。その結果、炎症反応を引き起こすことになり、周囲の細胞に対して害を及ぼす。このような細胞死を、ネクローシス(壊死)と呼ぶ。 米原らが発見したFas抗原(Fas)は、細胞内にアポトーシスのシグナルを伝達する細胞表層タンパク質である。Fasに対するモノクローナル抗体は、細胞に直接作用し、アポトーシスの形態をとる細胞死を誘導する。細胞傷害性T細胞からFasリガンドのcDNAクローニングが行われ、生体内には、アポトーシスを引き起こすために、Fasリガンドという作用分子とFasというレセプター分子がセットで存在していることが明らかとなった。 このFasとFasリガンドのシステムの生理的意味を考える上で重要なのは、SLEの自然発症モデルとして知られているlpr,gld,lprcgマウスがFasまたはFasリガンドの機能異常を有することを示した報告である。Fas抗原を介した細胞死誘導システムの異常は、自己免疫疾患を引き起こす原因のひとつとして示されたのである。現在では、Fas/Fasリガンドは、T細胞の発生や自己寛容の成立の過程で起こるアポトーシスに関与していると考えられている。また、Fasは非リンパ系組織でも発現しており、免疫系以外で重要な働きをしている可能性もある。 そこで、生体内におけるFasの機能をより深く解析するために、我々は、マウスFasに対するモノクローナル抗体を新たに作成し、それらを用いてin vitro、in vivoにおけるFasの生理機能を検討した。さらに、アポトーシス誘導能を有する抗Fasモノクローナル抗体を、自己免疫疾患のモデルマウスに投与する実験を行った結果、劇的な治療効果が得られることを明らかにした。この結果は、Fas/Fasリガンドのシステムが自己反応性T細胞やB細胞の除去に重要な働きをしていることを示しているだけでなく、Fasを介するアポトーシスを増強することが自己免疫疾患に対する新たな治療法となりえる可能性を示したものである。 【抗マウスFasモノクローナル抗体の作成】 マウスFasの細胞外領域と、可溶性のAic2-A(マウスIL-3レセプターの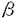 鎖)分子とのキメラ分子(可溶性マウスFas)を遺伝子工学の手法で作成し、モノクローナル抗体作成のための免疫源とした。Armenian hamsterまたはLewis ratに、可溶性Fasを免疫して得た脾臓細胞とマウスミエローマ細胞株NS-1とのハイブリドーマを定法に従って調製した。そして、マウスFasを高発現させたL5178Y-Fas細胞に特異的に結合する活性をサイトフルオロメトリー解析で同定することにより、抗Fasモノクローナル抗体を産生するハイブリドーマのスクリーニングを行った。その結果、細胞死を誘導する活性を有する抗体が2種類、細胞表面のFasを認識するが、細胞死は誘導しない抗体が6種類得られた。細胞死を誘導する抗体でFas陽性細胞を処理すると、DNAの断片化が誘導された。 鎖)分子とのキメラ分子(可溶性マウスFas)を遺伝子工学の手法で作成し、モノクローナル抗体作成のための免疫源とした。Armenian hamsterまたはLewis ratに、可溶性Fasを免疫して得た脾臓細胞とマウスミエローマ細胞株NS-1とのハイブリドーマを定法に従って調製した。そして、マウスFasを高発現させたL5178Y-Fas細胞に特異的に結合する活性をサイトフルオロメトリー解析で同定することにより、抗Fasモノクローナル抗体を産生するハイブリドーマのスクリーニングを行った。その結果、細胞死を誘導する活性を有する抗体が2種類、細胞表面のFasを認識するが、細胞死は誘導しない抗体が6種類得られた。細胞死を誘導する抗体でFas陽性細胞を処理すると、DNAの断片化が誘導された。 【活性化T細胞除去におけるFasシステムの関与】 T系列の細胞が生体内でアポトーシスを起こすと考えられるのは、胸腺と末梢である。胸腺内では、T細胞が分化成熟していく過程において、自己反応性の細胞や、不完全なT細胞受容体を有している細胞などが除去される段階(胸腺におけるポジティブ及び、ネガティブセレクション)でアポトーシスが誘導される。一方、末梢においては、末梢血中に存在する自己反応性T細胞(胸腺には存在しない自己抗原も末梢には存在している)が除去される段階や、抗原刺激により活性化された細胞が作用の収束とともに除去される段階などで、アポトーシスが誘導されると考えられる。活性化された細胞が除去されず、その作用が収束しないと、様々な免疫反応が惹起され続けることとなり、体内で慢性的な炎症状態が続くことになる。 生体内では、T細胞は抗原提示細胞、ウイルス感染細胞やがん細胞などによって活性化されると想定されるが、我々はスーパー抗原を用いたT細胞活性化のin vivoモデル実験系を考案し、実施した。スーパー抗原であるSEB(Staphilococcus enterotoxin Bacterium)は、ある種のT細胞受容体を持った細胞のみを特異的に活性化することが知られている。SEBと親和性の高いT細胞受容体であるV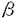 8を有する細胞が、特異的に活性化され、増殖するのである。そして興味深いことに、増加したV 8を有する細胞が、特異的に活性化され、増殖するのである。そして興味深いことに、増加したV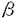 8陽性T細胞は、その後、数日で減少し、定常状態にもどる。この時起きる活性化細胞の除去に、Fasを用いた細胞死のシステムが関与しているかどうかを解析した。まず、V 8陽性T細胞は、その後、数日で減少し、定常状態にもどる。この時起きる活性化細胞の除去に、Fasを用いた細胞死のシステムが関与しているかどうかを解析した。まず、V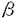 8陽性T細胞におけるFasの発現と機能を解析した。SEBを投与して3日後のマウスの脾臓T細胞では、V 8陽性T細胞におけるFasの発現と機能を解析した。SEBを投与して3日後のマウスの脾臓T細胞では、V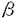 8陽性T細胞だけでFasの発現が高くなり、抗Fas抗体に対する感受性を獲得していることが明らかになった。また、Fasの発現がほとんどないlprマウスにおいては、SEB投与によるV 8陽性T細胞だけでFasの発現が高くなり、抗Fas抗体に対する感受性を獲得していることが明らかになった。また、Fasの発現がほとんどないlprマウスにおいては、SEB投与によるV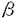 8T細胞の増加は、ワイルドタイプのマウスと同様に観察されたが、V 8T細胞の増加は、ワイルドタイプのマウスと同様に観察されたが、V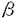 8T細胞の除去機構には、抑制がかかっていた。この結果は、マウスの生体内における活性化T細胞の除去にFasのシステムが関与していることを示すものである。 8T細胞の除去機構には、抑制がかかっていた。この結果は、マウスの生体内における活性化T細胞の除去にFasのシステムが関与していることを示すものである。 【自己免疫疾患モデルマウスに対する抗Fas抗体の治療効果】 生体内ではFas/FasLなどの発現が巧みに制御され、必要な時期や場において細胞死が引き起こされていると考えられる。自己免疫疾患では、このような細胞除去のシステムの一部が破綻していることが予想される。すなわち、自己反応性のT細胞やB細胞が除去されずに活動し続けていることが、自己免疫疾患の原因のひとつと考えられる。このような立場に立って考えると、Fasを介するアポトーシス誘導シグナルを増強することによって、自己免疫疾患を発症している個体で活動し続けている自己反応性細胞が除去できることが期待される。 我々の作成した抗Fas抗体は、Fasを発現しているリンパ球系の細胞に対して、強いアポトーシス誘導活性を有しているにも関わらず、肝毒性が低く、成熟個体に対しては、全く致死作用を示さなかった。そこで、これらの抗Fasモノクローナル抗体を、自己免疫疾患のモデルマウスであるMRL-gld/gldに投与し、リンパ腺症や自己免疫疾患が治癒するかを検討した。MRL-gld/gldマウスは、Fasリガンドに変異が存在する為に、生体内でFas/Fasリガンドの細胞死のシステムが機能しないことが原因で、自己免疫疾患の症状が発現しているマウスである。抗Fas抗体投与の結果、リンパ節、脾臓、胸腺に異常に集積するgld細胞が激減し、リンパ節の腫脹、脾臓の肥大が著しく抑制された。また、糸球体腎炎、唾液腺における動脈炎、肺炎などの炎症の程度が軽減した。さらに、関節の滑膜細胞の肥厚が抑制され、リウマチ様関節炎の症状が改善された。また血清中の自己抗体価も減少した。 このように、抗Fas抗体投与により、各疾患部位において劇的な治療効果が観察された。自己免疫疾患で見られる自己反応性T細胞やB細胞のような、慢性的に抗原刺激を受けている細胞は、Fasを介するアポトーシス誘導シグナルに高感受性となっていると考えられるので、FasリガンドのミュータントであるMRL-gld/gldマウスに限らず、自己免疫疾患の治療に抗Fas抗体が有効である可能性が期待される。実際、慢性的なT細胞の活性化により関節炎を起こしているHTLV-1/p40taxのトランスジェニックマウスに対して、この抗体を投与することで、症状の改善が見られている。 ここに示した治療実験は、抗体を用いることによって初めて可能となったものである。なぜなら、アポトーシス誘導能を有する可溶性Fasリガンドをマウスに投与すると、強い肝傷害を誘導すると報告されているからである。可溶性Fasリガンドは肝毒性が強いが、抗Fasモノクローナル抗体の場合には、抗体の種類によって標的細胞の特異性が異なり、肝毒性の程度が異なっている。ここに示した抗Fasモノクローナル抗体を用いた実験は、抗体を用いてFasを刺激する系を用いるなら、リンパ球特異的に強い細胞死のシグナルを誘導できることを示したものである。人の自己免疫疾患でも自己反応性リンパ球(慢性的に抗原刺激を受けている細胞)特異的にアポトーシスを誘導できる可能性が出てきたと我々は考えている。 【総括】 以上、免疫系におけるFas抗原の発現と機能について研究を進めてきた。本研究により、Fasによる細胞死のシステムは、末梢における活性化T細胞の除去に関与していることが明らかになった。さらに、自己免疫疾患モデルマウスに対する抗Fas抗体投与の実験結果から、生体内のFas抗原を刺激し、細胞死を誘導することは、自己免疫疾患の治療に有効であることが示された。 自己抗原に対する寛容の導入と、アポトーシスによるクローン除去の問題は、免疫学の中心的な課題の一つである。これらの問題について、数多くの研究がなされてきているが、その全体像は、まだ明らかになっていない。自己免疫疾患を克服するためには、まだ多くの解析がなされる必要があると思われるが、我々が行ったFasのシステムの研究は、自己免疫疾患の発症機構の解明や、その治療に新たな指針を与えるものであると考えることができる。Fasのシステムをさらに研究していくことによって、将来的には数多くの免疫疾患の発症機構が解明され、それらの有効な治療法につながっていくことが期待される。 |