ビタミンAの代謝産物であるレチノイン酸(RA)はヒト並びに他の哺乳類動物の成長や生命維持に必須の物質である。個体発生時には形態形成因子として、また成体においても分化・増殖に対して多岐にわたる作用を有することが知られている。近年の分子生物学の進歩に伴い、これらRAの多彩な作用が細胞の核内に存在するレチノイドレセプターを介して直接遺伝子の発現を制御することにより発揮されることが明らかになった。すなわち、リガンドの結合したレチノイドレセプターはダイマーを形成してDNAのホルモン応答部位に結合することにより、RNA Polymeraseによる転写が開始されてmRNAが伸張し、下流にある様々な遺伝子の発現を調節している。レチノイドレセプターは共通したドメイン構造を持つステロイド/サイロイドホルモンレセプターの一員であり、RAR及びRXRが知られており、それぞれ 、 、 、 、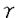 のサブタイプが存在する。現在までにRARsの病態発症・進展への関与がいくつか報告されており、急性前骨髄球性白血病(APL)ではRAR のサブタイプが存在する。現在までにRARsの病態発症・進展への関与がいくつか報告されており、急性前骨髄球性白血病(APL)ではRAR の異常が、頭頚部扁平上皮癌、肺癌ではRAR の異常が、頭頚部扁平上皮癌、肺癌ではRAR の異常が明らかにされている。一方、RAには角質化異常、脱毛、骨・軟骨代謝異常等の副作用も存在し、創薬の観点からは克服しなければならない問題点も抱えている。これら多岐にわたるレチノイドの詳細な作用機序の解明と臨床的応用の可能性を追求するにあたり、レセプターサブタイプ特異的なアンタゴニスト、アゴニスト創出の意義は極めて大きい。以上のことを鑑み探索研究に取り組んだ結果、筆者は強力なRARs選択的アンタゴニスト、RXRs選択的アゴニスト及びRAR の異常が明らかにされている。一方、RAには角質化異常、脱毛、骨・軟骨代謝異常等の副作用も存在し、創薬の観点からは克服しなければならない問題点も抱えている。これら多岐にわたるレチノイドの詳細な作用機序の解明と臨床的応用の可能性を追求するにあたり、レセプターサブタイプ特異的なアンタゴニスト、アゴニスト創出の意義は極めて大きい。以上のことを鑑み探索研究に取り組んだ結果、筆者は強力なRARs選択的アンタゴニスト、RXRs選択的アゴニスト及びRAR 選択的アゴニストの創出に成功した。 選択的アゴニストの創出に成功した。 RARs選択的アンタゴニストの創出 核内レセプターを介して様々な生理作用を発揮するレチノイドの作用機序を解明するためにアンタゴニストは極めて大きな力を発揮する。現在までにいくつかのRARアンタゴニストの報告があり、選択性に関して興味深い化合物は得られているものの活性面において満足すべきものはほとんどなく、より作用の強力なアンタゴニストが求められている。 筆者は、all-trans RA(ATRA)(1)や従来のレチノイドが持つ副作用の軽減化を指向してBASFのグループが合成した化合物2の構造に興味を持ち、アリール基間の回転制御が生物活性に影響を及ぼすのではないかと仮説を立て、脂溶性部とリンカー部を環で固定した4環性化合物3を合成したところ、非常に興味深い知見を得た。すなわち、ヒト前骨髄球性白血病細胞HL-60を用いたreceptor binding assay、分化誘導作用を指標としたin vitroスクリーニングの結果、3は2と同程度のbinding affinityを有するにも拘わらず、それ自身分化誘導作用は示さず、逆にATRAに対しアンタゴニスト作用を示すことが判明した。次にピラゾールN上置換基の効果を調べる目的で化合物4及び5を合成したところ、1-メチル異性体4のアンタゴニスト活性は3と比較して強くなったが、2-メチル異性体5ではほとんど活性が消失した。  そこで、これらの知見をもとにアンタゴニスト活性の向上を目指してさらなる化合物展開を図った結果、強力な作用を有する下記3化合物を見出した。 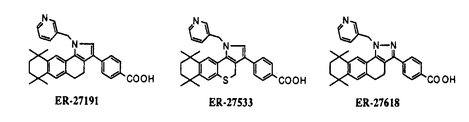 さらに、3化合物のうちの1つER-27191の特徴を精査した結果、ER-27191はRXRには結合せず、RARに幅広く結合し、in vivo経口投与によっても明確な作用を発揮する強力なアンタゴニストであることが判明した。 RXRs選択的アゴニストの創出 生理的なリガンドが9-cisレチノイン酸(9-cisRA)であるRXRsは同じファミリーに属する他のレセプターとヘテロダイマーを形成し、それぞれ固有のリガンドの機能を調節しているユニークなレセプターである。但し、9-cisRAはRXRsのみならずRARsにも結合するため、RXRsの詳細な作用機序解明にはRXRsに選択的に作用する化合物創出の意義は大きい。まだあまり数は多くないが、現在までにいくつかのRXRs選択的アゴニストが報告されており、興味深い臨床試験も行われている。 筆者は新規脂溶性部を探索する過程で、テトラヒドロキノリンを用いた化合物6ではRARsへの親和性が弱まり、RXRへの親和性が強くなるという現象を見出した。そこで、従来レチノイド様作用が発揮され難いために注目されていなかったN原子を導入した脂溶性部がRXRs選択的な化合物の創出に利用できるのではないか、また極性を高めることにより毒性の軽減にも繋がるのではないかと仮説を立て、本脂溶性部と9-cisRAのトリエン構造を組み合わせた化合物をデザインした。当初は9-cisRAのトリエン構造そのものを持つ化合物の構築を企てたが、中間体の不安定さから目的を達することはできなかった。そこで検討の結果、トリエン部6位にF原子を導入すると9-cisRA型の立体配置に保持された目的物が得られることが判明した。 7位置換基変換に焦点をあてて展開した化合物群の構造活性相関を調べた結果、エチル基を導入したER-35794がRXRs転写活性能及び選択性において最も優れ、本化合物は現在臨床への応用面で注目されているRXRsアゴニストLGD1069と比較して10倍以上のRXRs転写活性能を示した。  RAR 選択的アゴニストの創出 選択的アゴニストの創出 ATRAがその強力な分化誘導作用により驚異的な寛解率を示したAPLではレセプターサブタイプのうちRAR の異常が報告され、病態とRAR の異常が報告され、病態とRAR との密接な関係が明らかにされている。また、RAR との密接な関係が明らかにされている。また、RAR アゴニストAm80ではATRA耐性のAPL患者に対しても有効であることが示されている。一方、Am80がin vitroにおいて炎症性サイトカインであるIL-6の産生を抑制することが知られており、in vivoにおいても強力な抗炎症作用を発揮している。このように、RAR アゴニストAm80ではATRA耐性のAPL患者に対しても有効であることが示されている。一方、Am80がin vitroにおいて炎症性サイトカインであるIL-6の産生を抑制することが知られており、in vivoにおいても強力な抗炎症作用を発揮している。このように、RAR 選択的アゴニストはレチノイド作用のメカニズムを明らかにする手段に留まらず、それ自身疾病治療薬となる可能性を秘めている。加えて、選択性を高めることで毒性の軽減にも繋がり、RARに幅広く結合するレチノイドと比較して臨床においての有用性が期待できる。 選択的アゴニストはレチノイド作用のメカニズムを明らかにする手段に留まらず、それ自身疾病治療薬となる可能性を秘めている。加えて、選択性を高めることで毒性の軽減にも繋がり、RARに幅広く結合するレチノイドと比較して臨床においての有用性が期待できる。 Am80に代表される既存のRAR アゴニストはリンカー部にアミドを有することが構造的な特徴である。そこで筆者はアミド以外の基でRAR アゴニストはリンカー部にアミドを有することが構造的な特徴である。そこで筆者はアミド以外の基でRAR に選択性を持たせることができないかという考えのもとにサブタイプ別receptor binding assayを指標に新しい骨格の探索を行った。アミドプロトンに着目した変換を試みた結果、公知化合物であるが2、5-ジ置換ピロール体7がRAR に選択性を持たせることができないかという考えのもとにサブタイプ別receptor binding assayを指標に新しい骨格の探索を行った。アミドプロトンに着目した変換を試みた結果、公知化合物であるが2、5-ジ置換ピロール体7がRAR に比較的選択性が高いことを見出した。また、ATRAの脂溶性部を平面性の高いナフタレンで置換するとRAR に比較的選択性が高いことを見出した。また、ATRAの脂溶性部を平面性の高いナフタレンで置換するとRAR 選択性が高まるという実験事実を当時持ち合わせていたので、この知見を生かしてピロールとハイブリッド化した化合物8を合成したところ、このものはRAR 選択性が高まるという実験事実を当時持ち合わせていたので、この知見を生かしてピロールとハイブリッド化した化合物8を合成したところ、このものはRAR への親和性は弱いもののかなり高い選択性を示した。さらにレセプター親和性の向上を目指した新たな脂溶性部を探索した結果、高RAR への親和性は弱いもののかなり高い選択性を示した。さらにレセプター親和性の向上を目指した新たな脂溶性部を探索した結果、高RAR 選択性・転写活性能を示すベンゾフラン誘導体ER-50583、ER-65241を見出した。 選択性・転写活性能を示すベンゾフラン誘導体ER-50583、ER-65241を見出した。  これまで世界中で数多くのレチノイドが合成されてきたが、今回筆者は活性の強度や選択性の高さという観点から優れたRARsアンタゴニスト、RXRs選択的アゴニスト及びRAR 選択的アゴニストの創出に成功した。現在、アンタゴニストは社内外においてATRAで誘起される様々な生物活性の作用機序の解明に利用されている。RXRs選択的アゴニスト、RAR 選択的アゴニストの創出に成功した。現在、アンタゴニストは社内外においてATRAで誘起される様々な生物活性の作用機序の解明に利用されている。RXRs選択的アゴニスト、RAR 選択的アゴニストに関しては創出してまだ日が浅いため我々の手で更なる評価が必要であるが、先行品の動向を参考にして今後医薬品への応用を模索していきたいと考えている。 選択的アゴニストに関しては創出してまだ日が浅いため我々の手で更なる評価が必要であるが、先行品の動向を参考にして今後医薬品への応用を模索していきたいと考えている。 |