本研究は、血小板活性化因子(PAF)受容体の構造、細胞内情報伝達機構、および脱感作機構を明らかにする目的で、一連の解析を試みたものであり、下記の結果を得ている。 1.アフリカツメガエル卵母細胞を用いた遺伝子発現システムと電気生理学的な反応検出法を組み合わせた発現クローニング法を用いて、モルモット肺cDNAライブラリーからPAF受容体cDNAを単離した。cDNAから推定される受容体は342アミノ酸からなり、七回膜貫通構造を取る三量体G蛋白質連関型受容体ファミリーに属することが示唆された。 2.PAF受容体cDNAをChinese hamster ovary細胞に導入し、細胞内情報伝達機構を検討した。同細胞の膜画分はPAFを高親和性に結合し、100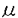 M GTP M GTP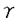 Sにより親和性の低下が観察され、同受容体が機能的にG蛋白質に連関することが示唆された。同受容体はまたリガンド依存性にIP3産生、アラキドン酸遊離、cAMP産生の抑制、42,44kDa MAPキナーゼの活性化等の作用を引き起こすことが示された。百日咳毒素(PTX)を用いた検討より、PAF受容体はPTX感受性、PTX非感受性のG蛋白質を介してこれらの作用と連関することが示唆された。 Sにより親和性の低下が観察され、同受容体が機能的にG蛋白質に連関することが示唆された。同受容体はまたリガンド依存性にIP3産生、アラキドン酸遊離、cAMP産生の抑制、42,44kDa MAPキナーゼの活性化等の作用を引き起こすことが示された。百日咳毒素(PTX)を用いた検討より、PAF受容体はPTX感受性、PTX非感受性のG蛋白質を介してこれらの作用と連関することが示唆された。 3.PAF受容体をアフリカツメガエル卵母細胞、およびChinese hamster ovary細胞に発現させ、受容体の同種脱感作および異種脱感作機構を検討した。PAF受容体をアフリカツメガエル卵母細胞に発現させ、PAFによるカルシウム依存性クロライドチャンネルの開口に対する非特異的セリン/トレオニンキナーゼ阻害剤H7の効果を検討したところ、H7はPAF受容体反応の終結を強く遅延させ、同時に同種脱感作を解除することが示された。ホスホリパーゼC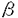 を活性化する野性型Gq を活性化する野性型Gq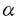 サブユニット、および恒常的活性型Gq サブユニット、および恒常的活性型Gq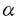 サブユニットをアフリカツメガエル卵母細胞に発現させ、PAF受容体からのカルシウム依存性クロライドチャンネルの開口を検討したところ、恒常的活性型Gq サブユニットをアフリカツメガエル卵母細胞に発現させ、PAF受容体からのカルシウム依存性クロライドチャンネルの開口を検討したところ、恒常的活性型Gq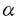 を発現した場合のみシグナルの遮断が生じ、同時に特異抗体で検出されるイノシトールリスリン酸(IP3)受容体蛋白質の減少、消失が起こることが判明した。この観察結果から、Gq連関受容体群の興奮はIP3受容体のダウンレギュレーションを介して広範な受容体を介するカルシウムシグナルを脱感作(異種脱感作)することが示唆された。 を発現した場合のみシグナルの遮断が生じ、同時に特異抗体で検出されるイノシトールリスリン酸(IP3)受容体蛋白質の減少、消失が起こることが判明した。この観察結果から、Gq連関受容体群の興奮はIP3受容体のダウンレギュレーションを介して広範な受容体を介するカルシウムシグナルを脱感作(異種脱感作)することが示唆された。 以上、本論文はPAF受容体の構造、細胞内情報伝達機構、および脱感作機構を明らかにした。本研究は、この分野の詳細な分子機構の解明へ重要な貢献をなすと考えられ、学位の授与に値すると考えられる。 |