学位論文要旨
| No | 214201 | |
| 著者(漢字) | 加藤,基浩 | |
| 著者(英字) | ||
| 著者(カナ) | カトウ,モトヒロ | |
| 標題(和) | エリスロポエチンのクリアランス機構 : 標的細胞のmigrationによるup-regulation | |
| 標題(洋) | ||
| 報告番号 | 214201 | |
| 報告番号 | 乙14201 | |
| 学位授与日 | 1999.03.10 | |
| 学位種別 | 論文博士 | |
| 学位種類 | 博士(薬学) | |
| 学位記番号 | 第14201号 | |
| 研究科 | ||
| 専攻 | ||
| 論文審査委員 | ||
| 内容要旨 | エリスロポエチン(EPO)は腎臓において産生される分子量約3万の糖タンパクであり、赤芽球系前駆細胞の分化、増殖作用を有する造血因子である。腎不全患者ではEPOの産生が充分行われず、多くの場合、貧血を呈する。遺伝子組換えEPOは、現在、この腎性貧血の治療に使用され、さらに各種貧血への適応が期待されている。前臨床、臨床におけるEPOの体内動態研究から、EPOの体内動態は非線形であることが示唆され、EPO反復投与により消失半減期が短縮するという報告もなされている。多くの生理活性ペプチドの体内動態はレセプター介在性エンドサイトーシス(RME)の飽和により非線形性を示すことが知られているが、EPOについては明らかでない。EPOの体内動態およびその変動要因を明らかにすることは、EPOの臨床での有効な使用法を考える上で極めて重要である。そこで、本研究の目的はEPOの体内動態の非線形メカニズムおよび反復投与時の変動機構を明らかにすることである。 SD系雄性ラットにEPOを0.2-5  再生不良性貧血といった造血障害時におけるEPOの体内動態を明らかにするために,stem cell factor receptorをコードするW遺伝子のmutationにより巨球性貧血を呈するW/WVマウスにおけるEPOの体内動態と正常マウス(+/+)における体内動態を比較した。+/+マウスでは,EPOの頻回投与により,大腿骨、脾臓におけるCLupは脾臓では0.48 EPOを反復投与した時の脾臓におけるCLupのup-regulation機構の解明を試みた。EPOレセプターはcolony forming unit-erythroid(CFU-E)に主に発現していることから、CFU-Eの数の変化とCLupの変化について検討した。EPOを2回投与後の脾臓中CFU-E数は,EPO処置量依存的に有意な増加を示した。CFU-E数とCLupとの間にほぼ原点を通る良い相関が認められたが、burst forming unit-erythroid(BFU-E)との間には有意な相関は認められなかった。さらにCFU-E数と脾臓細胞のEPO-bindingとの間にも良い相関関係が認められた。これらのことから脾臓におけるCLupの増加は細胞当たりのレセプター数の増加ではなく、標的細胞であるCFU-Eの増加によるものであることが明らかになった。 骨髄、脾臓におけるup-regulationの懸かり方の違いがCFU-Eが骨髄から脾臟へ移行したことに起因するという仮説を立て、検証を試みた。111In-EPOはRMEによりCFU-Eに取り込まれ、111Inは細胞内の鉄結合性タンパクに結合するため、CFU-Eを111Inにより標識できると考えた。111In-EPO投与しCFU-Eを標識した後、過剰量のEPO投与により骨髄中放射能は、対照群に比べ,有意に減少した。一方,脾臓中放射能も,対照群に比べ有意に減少した。このことから上記の仮説は否定され、骨髄中CFU-Eの脾臓への移行が促進されたためではないことが示唆された。新たに、骨髄中のBFU-Eが、脾臓に移行し、そこでCFU-Eに分化したという仮説を立てた。3H-thymidine投与により増殖細胞を標識し、細胞の動態を調べた結果、骨髄中放射能は過剰量のEPO投与により対照群に比べ,有意に減少し、脾臓中放射能はEPO投与により対照群に比べ,有意に増加した。3H-thymidine標識された脾臓細胞をPercollにより分画した結果、処置1、2日後の脾臓ではBFU-Eに相当する分画の放射能が対照群に比べ増加していたが、CFU-Eに相当する分画の放射能の増加はわずかであった(図2)。処置3、4日後では、BFU-Eに相当する分画の放射能の増加はわずかであり、CFU-Eに相当する分画の放射能の増加が認められ、BFU-Eが脾臓に移行し、CFU-Eに分化したと考えられた(図2)。BFU-Eが脾臓に移行することを確認するため、BFU-E画分の細胞をラットに投与し、その分布を調べた結果、BFU-Eは脾臓に特異的に移行することが示唆された。これらの結果から、EPO処置により先ず骨髄中のBFU-Eが血液中に放出され、脾臓に移行し、脾臓でCFU-Eに分化、増殖し、その結果としてCFU-Eが増加し、EPOレセプターが増加することにより、125I-EPOのCLupの増加が認められたと考えられた。 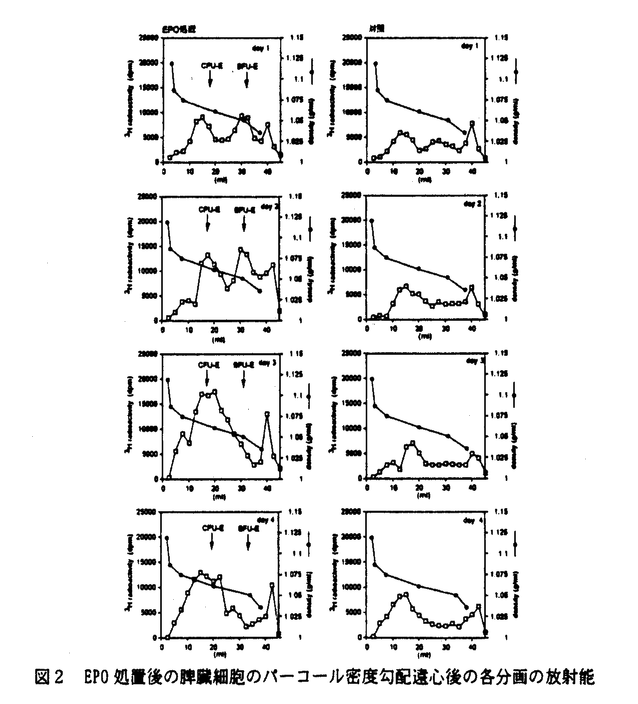 125I-EPOを週1回4回皮下投与した際,10例中8例のラットで,4回目投与時の血漿中濃度はほとんど検出されなかったが,残り2例は対照ラットと同等かそれ以上の増加がみられた。すべての個体で抗体が検出され、2例ではいずれも残り8例よりも抗体量が少なかった。種々の量のラット抗EPO抗血清をラットに静脈内投与した後,125I-EPOを0.1 ラット、マウスにおける体内動態研究より、EPOの非線形クリアランス機構はKm値がEPOレセプターのKd値に類似していること、骨髄、脾臓における組織取り込みのdown-regulationおよびup-regulationが認められること、レセプターを持つCFU-E数と組織取り込みクリアランスが相関することからEPOレセプターを介したレセプター介在性エンドサイトーシスによることが明らかになった。さらに、EPOによりBFU-Eのmigrationが促進され、このmigrationに起因するEPOレセプターのup-regulationに臓器間差が見られることが明らかになった。EPOがEPO自身のクリアランスの変動因子になっていることが示された。また、抗体が産生された場合、抗体がEPOの体内動態にbiphasicな影響を与えることが明らかになった。 | |
| 審査要旨 | エリスロポエチン(EPO)は腎臓において産生される分子量約3万の糖タンパクであり、赤芽球系前駆細胞の分化、増殖作用を有する造血因子である。前臨床、臨床におけるEPOの体内動態研究から、EPOの体内動態は非線形であることが示唆され、EPO反復投与により消失半減期が短縮するという報告もなされている。多くの生理活性ペプチドの体内動態はレセプター介在性エンドサイトーシス(RME)の飽和により非線形性を示すことが知られているが、EPOについては明らかでない。EPOの体内動態およびその変動要因を明らかにすることは、EPOの臨床での有効な使用法を考える上で極めて重要である。本研究の目的はEPOの体内動態の非線形メカニズムおよび反復投与時の変動を明らかにすることである。 SD系雄性ラットにEPOを各種投与量で単回あるいは定速静脈内投与した時の全身クリアランス(CLtotal)は投与量の増加により減少し、非線形が認められ、線形消失とMichaelis-Menten型の消失により解析した結果、Michaelis定数(Km値)は219pMであり、EPOレセプターの解離定数(Kd値)に類似するものであった。血漿中濃度および組織中濃度から組織取り込みクリアランス(CLup)を算出した。骨髄、脾臓におけるCLupは、飽和現象を示し、Km値(約250-450pM)は血漿中濃度推移から求められたKm値に類似した値を示した。血漿中濃度推移で認められる非線形性は骨髄、脾臓への取り込みの飽和に起因することが示唆された。EPOを皮下投与後の125I-EPOの骨髄、脾臓におけるCLupは低下し、down-regulationが認められた。EPOを2回静脈内投与したラットの骨髄、脾臓のCLupは、骨髄、脾臓ともにEPO処置量の増加に従い、CLupの増加(up-regulation)が認められ、脾臓において顕著であった。EPO処置ラットに125I-EPOを静脈内投与した時の血漿中放射能の消失半減期はEPO処置量の増加に従い、有意に短縮した。EPO処置によるヘマトクリット値、CLupの変化の間には、良い相関関係が認められた。以上より、標的臓器のレセプターがEPOの非線形体内動態に重要な役割をはたしていることが示唆された。 さらに、再生不良性貧血といった造血障害時におけるEPOの体内動態を明らかにするために,stem cell factor receptorをコードするW遺伝子のmutationにより巨球性貧血を呈するW/WVマウスにおけるEPOの体内動態と正常マウス(+/+)における体内動態を比較した。両マウスともに骨髄,脾臓のCLupは類似したKm値をもつ飽和を示したが、最大速度はW/WV/マウスで低いを示した。W/WVマウスと+/+マウスでEPOの頻回投与による組織取込みのup-regulationの懸かり方が異なることが明らかになった。両マウスの骨髄と脾臓のCLupの和とHct値の関係は同一の直線上にプロットされた。この結果から正常マウスばかりでなく貧血マウスにおいても薬理レセプターが組織取込みに働いていることが示唆された。 EPOを反復投与した時の脾臓におけるCLupのup-regulation機構の解明を試みた。EPOレセプターはcolony forming unit-erythroid(CFU-E)に主に発現していることから、CFU-Eの数の変化とCLupの変化について検討した。EPO処置後の脾臓中CFU-E数は,EPO処置量依存的に有意な増加を示した。CFU-E数とCLupとの間にほぼ原点を通る良い相関が認められたが、burst forming unit-erythroid(BFU-E)との間には有意な相関は認められなかった。脾臓におけるCLupの増加は、標的細胞であるCFU-Eの増加によるものであることが明らかになった。 骨髄、脾臓におけるup-regulationのかかり方の違いがCFU-Eが骨髄から脾臓へ移行したことに起因するという仮説を立て、検証を試みた。111In-EPOを投与しRMEによりCFU-Eを特異的に標識した。過剰量のEPO投与により骨髄中放射能は、対照群に比べ,有意に減少した。一方,脾臓中放射能も,対照群に比べ有意に減少し、先の仮説は否定された。新たに、骨髄中のBFU-Eが、脾臓に移行し、そこでCFU-Eに分化したという仮説を立てた。3H-thymidine投与により増殖細胞を標識し、細胞の動態を調べた結果、骨髄中放射能は過剰量のEPO投与により対照群に比べ,有意に減少し、脾臓中放射能はEPO投与により対照群に比べ,有意に増加した。3H-thymidine標識された脾臓細胞をPercollにより分画した結果、処置1、2日後の脾臓ではBFU-Eに相当する分画の放射能が対照群に比べ増加していたが、CFU-Eに相当する分画の放射能の増加はわずかであった。処置3、4日後では、BFU-Eに相当する分画の放射能の増加はわずかであり、CFU-Eに相当する分画の放射能の増加が認められ、BFU-Eが脾臓に移行し、CFU-Eに分化したと考えられた。これらの結果から、EPO処置により先ず骨髄中のBFU-Eが血液中に放出され、脾臓に移行し、脾臓でCFU-Eに分化、増殖し、著しくCFU-Eが増加し、EPOレセプターが増加することにより、125I-EPOのCLupの増加が認められたと考えられた。 種々の量のラット抗EPO抗血清をラットに静脈内投与した後,125I-EPOを0.1 以上、EPOの非線形クリアランス機構および変動機構を明らかにした。特にレセプターのup-regulationが細胞のmigrationに起因するという知見は初めてのものであり興味ある現象である。これらEPOの体内動態を明らかにしたことは、EPOの有効かつ安全な使用法を考える上において貴重な知見であり、博士(薬学)の学位を授与するに値するものと認めた。 | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/51110 |
 g/kg単回あるいは16-1600ng/kg/hの速度で定速静脈内投与した時の全身クリアランス(CLtotal)は投与量の増加により減少し、非線形が認められ、線形消失とMichaelis-Menten型の消失を考慮した解析の結果、Michaelis定数(Km値)は219pMであり、EPOレセプターの解離定数(Kd値)に類似するものであった。125I-EPO単回静脈内投与30分後の血漿、骨髄、脾臓中濃度を測定し、血漿中濃度および組織中濃度から組織取り込みクリアランス(CLup)を算出した。骨髄、脾臓におけるCLupは血漿中初期濃度の増加に従い、減少し、飽和現象が認められた。CLupのKm値(約240-450pM)は血漿中濃度推移から求められたKm値に類似した値を示した。血漿中濃度推移で認められる非線形性は骨髄、脾臓への取り込みの飽和に起因することが示唆された。EPOを皮下投与後の125I-EPOの骨髄、脾臓におけるCLupは低下し、down-regulationが認められた。EPOを1日おきに2回静脈内投与したラットの骨髄、脾臓のCLupは、骨髄、脾臓ともにEPO処置量の増加に従った増加が認められ、脾臓において顕著であった(図1)。このCLupの増加は飽和性の取り込みの増加によるものであった。EPO処置ラットに125I-EPO0.2
g/kg単回あるいは16-1600ng/kg/hの速度で定速静脈内投与した時の全身クリアランス(CLtotal)は投与量の増加により減少し、非線形が認められ、線形消失とMichaelis-Menten型の消失を考慮した解析の結果、Michaelis定数(Km値)は219pMであり、EPOレセプターの解離定数(Kd値)に類似するものであった。125I-EPO単回静脈内投与30分後の血漿、骨髄、脾臓中濃度を測定し、血漿中濃度および組織中濃度から組織取り込みクリアランス(CLup)を算出した。骨髄、脾臓におけるCLupは血漿中初期濃度の増加に従い、減少し、飽和現象が認められた。CLupのKm値(約240-450pM)は血漿中濃度推移から求められたKm値に類似した値を示した。血漿中濃度推移で認められる非線形性は骨髄、脾臓への取り込みの飽和に起因することが示唆された。EPOを皮下投与後の125I-EPOの骨髄、脾臓におけるCLupは低下し、down-regulationが認められた。EPOを1日おきに2回静脈内投与したラットの骨髄、脾臓のCLupは、骨髄、脾臓ともにEPO処置量の増加に従った増加が認められ、脾臓において顕著であった(図1)。このCLupの増加は飽和性の取り込みの増加によるものであった。EPO処置ラットに125I-EPO0.2 ),MRTは有意に延長し,CLtotalは減少した。さらに抗EPO抗血清の投与量を増加させるとT1/2(
),MRTは有意に延長し,CLtotalは減少した。さらに抗EPO抗血清の投与量を増加させるとT1/2(