本研究はぶどう膜炎における視細胞障害に対する一酸化窒素(NO)の関与について検討したものである。過去にぶどう膜炎の動物実験モデルにおいて、誘導型一酸化窒素合成酵素(NOS-2)を発現しているマクロファージが視細胞外節に局在する事が報告されており、本研究では視細胞外節に局在する網膜自己抗原のマクロファージ活性能について培養マクロファージを用いた検討を行っている。また、マウスの実験的自己免疫性ぶどう膜炎にNOS-2の選択的阻害剤であると考えられているaminoguanidineを投与し、視細胞障害に対する影響を検討している。本研究では、下記の結果が得られている。 1.マクロファージを網膜自己抗原、合成ペプチドと共に培養し、培養上清中のnitrite濃度をNO産生の指標としてGriess反応を用いて測定したところ、RAW 264.7において網膜S抗原とIRBPは1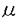 g/mlから50 g/mlから50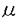 g/mlの濃度で容量依存的にnitrite産生を誘導したが、ロドプシン、リカバリン、フォスデューシンなどの網膜自己抗原やmyelin basic proteinはnitrite産生を誘導しなかった。また、2-6-11モチーフを含む合成ペプチドとコントロールの合成ペプチドによる誘導されたnitrite産生量に有意差は認められなかった。NOS-2を比較的選択的に阻害すると考えられているaminoguanidineやチロシンキナーゼの阻害剤であるgenisteinはS抗原により誘導されたRAW 264.7のNO産生を阻害した。ラットのチオグリコレート誘発腹腔内マクロファージにおいてもS抗原とIRBPはnitrite産生を誘導したが、有色家兎のチオグリコレート誘発腹腔内マクロファージにおいては両者ともnitrite産生を誘導しなかった。 g/mlの濃度で容量依存的にnitrite産生を誘導したが、ロドプシン、リカバリン、フォスデューシンなどの網膜自己抗原やmyelin basic proteinはnitrite産生を誘導しなかった。また、2-6-11モチーフを含む合成ペプチドとコントロールの合成ペプチドによる誘導されたnitrite産生量に有意差は認められなかった。NOS-2を比較的選択的に阻害すると考えられているaminoguanidineやチロシンキナーゼの阻害剤であるgenisteinはS抗原により誘導されたRAW 264.7のNO産生を阻害した。ラットのチオグリコレート誘発腹腔内マクロファージにおいてもS抗原とIRBPはnitrite産生を誘導したが、有色家兎のチオグリコレート誘発腹腔内マクロファージにおいては両者ともnitrite産生を誘導しなかった。 2.網膜S抗原によるNF-kBの活性化をelectrophoretic mobility shift assayにより検出した。NF-kB活性化は網膜S抗原による刺激後30分から120分の間認められ、NF-kB阻害剤(PDTC)、チロシンキナーゼ阻害剤(Herbimycin A)、MAPキナーゼ阻害剤(PD98059)、プロテインキナーゼC阻害剤(GF109203X)はNF-kB活性化を阻害した。 3.網膜自己抗原によるマクロファージのスーパーオキシド産生をチトクロームC法を用いて測定した。有色家兎のチオグリコレート誘発腹腔内マクロファージにおいて網膜S抗原はスーパーオキシド産生を誘導したが、IRBPにはこの誘導能は認められなかった。ラットのチオグリコレート誘発腹腔内マクロファージはS抗原の刺激により少量のスーパーオキシドを生成し、RAW 264.7においてはS抗原、IRBPともスーパーオキシド産生を誘導しなかった。 4.マウスの実験的自己免疫性ぶどう膜炎において、NOS-2の選択的阻害剤であるaminoguanidineを腹腔内に投与した治療群とPBSを投与した対照群において病理組織の視細胞層の厚さを測定し比較したところ、治療群にて有意に視細胞層は厚くなっており、aminoguanidineの視細胞障害に対する治療効果が認められた。 以上、本論文は、網膜視細胞層に局在する網膜自己抗原が培養マクロファージにおいて一酸化窒素産生を誘導することを明らかにし、NOS-2の阻害剤がマウスの実験的自己免疫性ぶどう膜炎において視細胞障害を軽減することを明らかにした。本研究はぶどう膜炎における視細胞障害のメカニズムの解明に重要な貢献をなすと考えられ、学位の授与に値するものと考えられる。 |