卵白は、ゲル形成能、保水性、結着性、起泡性、乳化性などの多用な機能をもつため様々な食品に利用されている。とりわけ、ゲル形成能、保水性および結着性は、魚肉すり身加工品、畜肉加工品、製麺、製菓、製パンさらにはフライなどの揚げ物などに応用されており、好ましい食感や色調を提供し、卵白はそれら加工品において不可欠な副原料となっている。しかしながら、卵白のゲル形成機構や保水性を高める作用機序については不明な点が多く、上述したような卵白のもつ食品的な機能特性をさらに発展させて応用するまでには至っていない。 本研究はこのような背景の下、まず、卵白の加熱ゲル化に及ぼすpHの影響を明らかにすることを試みた。次に、メイラード反応を用いて卵白の加熱ゲル形成能を向上させることを試み、さらに卵白フィルムの形成機構を検討しその物性の強化方法を探索したもので、得られた成果の大要は以下の通りである。 1.の卵白のpH調整による加熱ゲル改変 まず、卵白構成タンパク質の加熱に伴う変化を種々のpHで調べた。卵白タンパク質溶液の調製にあたっては、生卵白にタンパク質濃度が0.2%となるように適量の水を加えた後、同液に対して透析し無機塩類および糖質を除去した。この卵白溶液に等量のpH3、5、7、9および11の40mMクエン酸-リン酸緩衝液を加え、種々のpHの0.1%卵白タンパク質溶液を調製した。次いで、これら溶液を25℃から95℃まで1.5℃/分で昇温加熱し、濁度、表面および総SH基含量、円偏光二色性(CD)の変化を測定した。 その結果、卵白タンパク質溶液は、主成分オボアルブミン(全卵白タンパク質の54%)とオボトランスフェリン(同35%)の等電点に近いpH5および7で、加熱に伴い凝集が生じ、65℃付近から濁度は上昇し始めた。一方、pH3、9および11の試料は加熱上限温度95℃まで透明であった。そこで濁度の生じないこれら3試料につき、CD分析で222nmの分子楕円率の変化パターンを調べた。その結果、卵白タンパク質の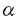 -ヘリックスが急激に崩壊し始める温度を指標とした二次構造の安定性は、pH3<11<9の順に高かった。また、表面SH基含量の変化パターンからみた卵白タンパク質の三次構造の安定性は、pH3<11<5<7=9であった。以上のように、pH3および11の試料では、pH5および7のものより三次構造の熱安定性が低いにもかかわらず加熱上限温度95℃まで濁度が生じなかったが、その原因として前二者のpHで分子間斥力が大きかったことが考えられた。さらにpH11では加熱により総SH基含量が増大し、分子内SS結合の開裂が示唆された。 -ヘリックスが急激に崩壊し始める温度を指標とした二次構造の安定性は、pH3<11<9の順に高かった。また、表面SH基含量の変化パターンからみた卵白タンパク質の三次構造の安定性は、pH3<11<5<7=9であった。以上のように、pH3および11の試料では、pH5および7のものより三次構造の熱安定性が低いにもかかわらず加熱上限温度95℃まで濁度が生じなかったが、その原因として前二者のpHで分子間斥力が大きかったことが考えられた。さらにpH11では加熱により総SH基含量が増大し、分子内SS結合の開裂が示唆された。 次に、卵白加熱ゲルの物性に及ぼすpHの影響をみるために、卵白に6N塩酸または6N水酸化ナトリウム溶液、および水を加えて、pH3、5、7、9および11の9%卵白タンパク質溶液を調製した。次に、本試料を80℃、40分間処理し加熱ゲルを作製した。さらに本加熱ゲルを二重押し込み試験に供し、硬さ、弾力性、付着性、咀嚼性を調べて物性を評価し、また別途試験により保水性を調べた。 硬さはpH3=7<5=9<11、弾力性はpH3<5=7<9=11、付着性はpH3<9<7<5<11、咀嚼性はpH3<7=9<5<11の順に高く、pH11のゲル物性が最も優れていると判断された。一方、本加熱ゲルの保水性はpH5<7<3<9=11の順に高く、試料のpHがオボアルブミンやオボトランスフェリンの等電点から離れるほど高くなる傾向を示した。 SDSおよび2-メルカプトエタノールを添加して加熱ゲルを調製した試験より、その保水性にはタンパク質のアンフォールディングおよび付随して生ずる分子間SS結合が重要な働きをすることが示唆された。さらに、走査型および透過型電子顕微鏡による加熱ゲルの微細構造観察より、pH11の試料で最も均一なネットワーク構造が示され、この結果は本試料の優れた物性や保水性の高さとよく相関した。 2.乾燥卵白のメイラード反応による加熱ゲル改変 卵白には0.4%程度の遊離グルコースが含まれている。一方、商業的乾燥卵白では、脱糖と称して、乾燥に先立ち酵母を添加してグルコースを除去し、保存中のメイラード反応による褐変および不溶化を防ぐ。そこで本研究では、未脱糖乾燥卵白を不溶化しない程度の温和な条件、すなわち55℃、相対湿度35%の雰囲気下で12日間保蔵し種々の試験に供した。その結果、乾燥卵白はわずかに褐変し、対応して卵白中の遊離グルコースおよびタンパク質の遊離アミノ基が減少した。さらに2-メルカプトエタノール存在下および非存在下でのSDS-PAGE分析で、主要卵白タンパク質の分子量は増加し、卵白タンパク質とグルコースとの結合が示唆された。以上の結果から、12日間の保蔵で未脱糖乾燥卵白にメイラード反応が起きたことが示された。この間、卵白タンパク質の表面SH基含量は2.02から9.88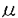 mol/g proteinまで増大し、 mol/g proteinまで増大し、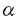 -ヘリックス含量も27.3%から25.9%へとわずかに減少した。したがって、メイラード反応の影響は三次構造の変化とともに、より安定な二次構造の変化をも伴うものであることが明らかになった。また、先のSDS-PAGE分析から、卵白タンパク質は可溶性の凝集体を形成していること、およびこの変化にはSS結合とその他の共有結合が関与していることが示唆された。 -ヘリックス含量も27.3%から25.9%へとわずかに減少した。したがって、メイラード反応の影響は三次構造の変化とともに、より安定な二次構造の変化をも伴うものであることが明らかになった。また、先のSDS-PAGE分析から、卵白タンパク質は可溶性の凝集体を形成していること、およびこの変化にはSS結合とその他の共有結合が関与していることが示唆された。 次に、上述の12日間保蔵した未脱糖乾燥卵白から、2N水酸化ナトリウム溶液および水を加えて固形分含量10%でpH9の卵白溶液(タンパク質濃度9.0%)を調製し、80℃、40分間処理して加熱ゲルを調製した。 本加熱ゲルは、調製直後の未脱糖乾燥卵白のそれと比べ、物性測定による破断強度および破断距離は、それぞれ5.6および1.7倍になり、保水性は88.6%から96.1%に上昇した。さらに、この加熱ゲルの物性および保水性は、メイラード反応を起こした卵白タンパク質の表面SH基含量とは正の、逆に残存する総SH基含量とは負の相関を示した。なお、脱糖乾燥卵白を上述した条件下で12日間保藏しても、未脱糖乾燥卵白の場合のような変化は認められなかった。 3.卵白フィルムの機能強化 乾燥卵白(Henningsen Foods社製P-39、固形分92%以上、タンパク質80%以上)9gに水100mLおよび可塑剤のポリエチレングリコール5.4gを加え、2N水酸化ナトリウム溶液でpH10.5、11.0および11.5に調整した。次に、本試料および40℃、30分間の加熱処理した試料をテフロンコーティングしたガラス板(21×35cm)に展開し、25℃、相対湿度50%の雰囲気下で乾燥させ、厚さ130±13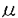 mのフィルムを調製した。 mのフィルムを調製した。 pH10.5、11.0および11.5の試料展開液の表面SH基含量は、当初それぞれ3.81、6.72および12.85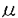 mol/g proteinであったが、加熱によってそれぞれ5.07、9.36および19.45 mol/g proteinであったが、加熱によってそれぞれ5.07、9.36および19.45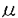 mol/g proteinに変化した。次に、作製した卵白フィルムの引っ張り強度、引っ張り伸び、および水への溶解性を測定したところ、展開液の卵白タンパク質表面SH基含量と、卵白フィルムの引っ張り強度および引っ張り伸びとは正の、逆に水への溶解性とは負の相関が示された。 mol/g proteinに変化した。次に、作製した卵白フィルムの引っ張り強度、引っ張り伸び、および水への溶解性を測定したところ、展開液の卵白タンパク質表面SH基含量と、卵白フィルムの引っ張り強度および引っ張り伸びとは正の、逆に水への溶解性とは負の相関が示された。 次に、架橋剤のダイアルデヒドスターチ、さらにオレイン酸を前述した試料溶液に添加し、2N水酸化ナトリウム溶液でpH11.3に調製後、45℃、20分間の加熱処理を行なった。次いで、上述したように卵白フィルムを作製し、それらの引っ張り強度、引っ張り伸び、および水への溶解性を調べた。 ダイアルデヒドスターチおよびオレイン酸の添加で引っ張り強度および引っ張り伸びは増加し、逆に水への溶解性は減少した。ダイアルデヒドスターチの効果は対乾燥卵白5%で最大となった。なお、2-メルカプトエタノール存在下でのSDS-PAGE分析から、ダイアルデヒドスターチは卵白タンパク質を共有結合により架橋することが示された。また、対乾燥卵白10%のオレイン酸の効果もダイアルデヒドスターチとほぼ同じ傾向を示した。オレイン酸の場合、フィルム展開液のSDS非存在下でのnative PAGEの結果から、卵白タンパク質に負の電荷を付加することが示され、分子間の斥力がフィルム化に重要と考えられた。さらに、オレイン酸は卵白タンパク質のSH基を表面に露出させることが明らかになり、空気酸化による分子間SS結合がフィルムの機能強化につながることが推察された。 以上、本研究により、まず、卵白加熱ゲルの物性および保水性はpH11のときに最も優れていることが明らかとなった。このpHでは加熱に伴い卵白タンパク質表面SH基が顕著に増大し、その増大が加熱ゲルの優れた物性や高い保水性の発現に重要と考えられた。さらに、卵白フィルムの優れた物性の発現や、水への溶解性の減少にも、フィルム展開液の卵白タンパク質表面SH基の増大が関与した。また、乾燥卵白のタンパク質表面SH基の増大には、メイラード反応、アルカリ処理、およびオレイン酸の添加が効果的であった。以上、本研究は、卵白のゲル化機構の一端を明らかにしたもので、その成果は食品化学上に資するのみならず、優れた加工食品の開発につながるもので応用面にも寄与するところが大きいものと思われる。 |