カルボラン(dicarba-closo-dodecaboranes,C2B10H12)は炭素原子2個を含む二十面体ホウ素クラスター構造を有し、26個の骨格電子の電子非局在化により安定化された化合物である。その特異な構造と性質は、無機化学、高分子化学、材料科学分野で注目を集めている。一方、医薬化学分野でも、癌の中性子捕捉療法(NCT:Neutron Capture Therapy)への応用が盛んに検討されている。天然のホウ素同位体の約20%を占める10Bの低エネルギー中性子による崩壊によるエネルギーが一つの細胞を破壊するのに相当する強度であることから、癌細胞に特異的に取り込ませることが可能となれば、中性子線の照射により周囲の正常細胞に影響を与えずに有効な治療法となりうる。そこで、カルボラン骨格をアミノ酸、核酸等に結合し、さらに膜透過性や癌細胞への選択的取込みを考慮した分子の設計が行われてきた。 これらの中性子捕捉療法への応用に比べ、カルボラン骨格の物理的、化学的性質を利用して生物活性物質の部分構造として応用しようとする試みは為されていない。本研究は、受容体に認識される構造として、カルボランを分子設計に応用する初の試みを行ったものである。本研究に応用するカルボラン骨格の性質は嵩高い球状の形状と高い疎水性であり、それを核内受容体リガンドの疎水性ファーマコフォアとして用いて活性化合物を設計することが本研究の基本概念である。疎水性相互作用は水素結合等と共に、リガンドー受容体の安定化に極めて重要な要因であり、疎水性ファーマコフォアの生物活性に与える影響は大きいものである。また、カルボランは炭素の位置により、o-,m-,p-の三種の異性体が存在し、炭素上の置換基の変換により多彩な分子設計が可能である。 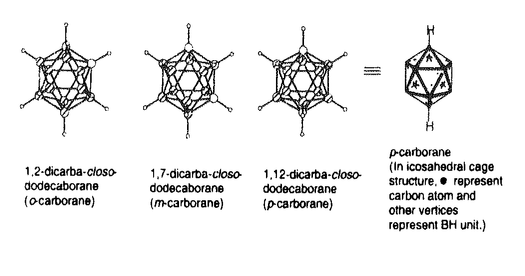 図表 図表 本研究ではカルボランの物理的、化学的性質を利用し、第一に核内受容体レチノイン酸レセプター(RAR)リガンドの設計と合成、活性評価を行っている。坐体内リガンドであるレチノイン酸はRARへの結合を介して、RARとレチノイドXレセプター(RXR)とのヘテロダイマーが標的遺伝子のホルモン応答配列に結合した後、その転写を制御する。レチノイン酸及び代表的合成レチノイドであるAm80の構造活性相関により、レチノイドの活性発現には、カルボン酸とそれに対して適切な空間配置にある嵩高い疎水性領域が必要である。そこで、Am80の疎水性領域としてカルボラン骨格を導入した誘導体を種々、設計、合成し、その活性をヒト前骨髄性白血病細胞HL-60の分化誘導能により評価したところ、ベンゼン環のp-位にカルボラン骨格を導入した化合物BR201が、レチノイド拮抗作用を示すこと見い出した。さらに、同化合物の構造検討により、カルボン酸と疎水性領域の距離を短縮したジフェニルアミン誘導体を設計、合成し、顕著なレチノイド活性を見い出した。中でも、化合物BR403は生体内リガンドであるレチノイン酸に匹敵する強力な活性を示した。  図表 図表 第二に、核内受容体エストロゲン受容体(ER)リガンドのの設計と合成、活性評価を行っている。生体内リガンドである17 -estradiolはERへの結合を介して、ERのホモダイマーが標的遺伝子のホルモン応答配列に結合した後、その転写を制御する。エストロゲンの活性発現には、フェノール性水酸基、それに対して適切な空間配置にある水酸基、そして、それらの配置を規定する嵩高い疎水性構造が必要である。そこで、カルボラン骨格をステロイドC、D環に対応させる一連のカルボラン含有エストロゲンを設計、合成した。 -estradiolはERへの結合を介して、ERのホモダイマーが標的遺伝子のホルモン応答配列に結合した後、その転写を制御する。エストロゲンの活性発現には、フェノール性水酸基、それに対して適切な空間配置にある水酸基、そして、それらの配置を規定する嵩高い疎水性構造が必要である。そこで、カルボラン骨格をステロイドC、D環に対応させる一連のカルボラン含有エストロゲンを設計、合成した。  図表 図表 ERを介した転写活性化をルシフェラーゼレポータージーンアッセイにより、活性を評価したところ、設計した化合物には強いエストロゲン活性が認められ、特に、化合物BE120は生体内リガンドである17 -estradiolに比べ10倍以上の活性を示した。この活性は、ER -estradiolに比べ10倍以上の活性を示した。この活性は、ER を用いた[3H]-17 を用いた[3H]-17 -estradiol結合競合試験においても確認された。また、これらの実験事実はER -estradiol結合競合試験においても確認された。また、これらの実験事実はER と17 と17 -estradiolとの複合体X線結晶解析の座標への計算化学によるドッキングによってもカルボランの形状の受容体疎水空間へのフィットにより説明できることを明らかにしている。 -estradiolとの複合体X線結晶解析の座標への計算化学によるドッキングによってもカルボランの形状の受容体疎水空間へのフィットにより説明できることを明らかにしている。 本研究により、カルボラン骨格の立体的形状と疎水性を、生理活性物質の疎水性ファーマコフォアとして応用できることを明らかにするとともに、その合成を通じてカルボランの合成化学的な応用についても新しい知見を得ている。 以上、飯嶋 徹の研究成果は、有機化学、医薬化学研究に資するところ大であり、博士(薬学)の学位を授与するに十分なものと認めた。 |